摘要:14.高铁酸钠是一种新型.高效.多功能水处理剂. 湿法制备的主要反应方程为:2Fe(OH)3+3ClO―+4OH―=2FeO42-+3Cl―+5H2O 干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4 下列有关说法不正确的是 A.高铁酸钠中铁显+3价 B.湿法中每生成1mol Na2FeO4转移3 mol电子 C.干法中每生成1mol Na2FeO4转移4 mol电子 D.Na 2FeO4处理水时消毒杀菌的原理与HClO相同
网址:http://m.1010jiajiao.com/timu3_id_397304[举报]
2012年3月22日是第二十届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的 倍.
(2)自来水厂常用高铁酸钠(Na2FeO4,强氧化剂)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理 .
(3)某无色废水中可能含有Fe2+、Al3+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图所示: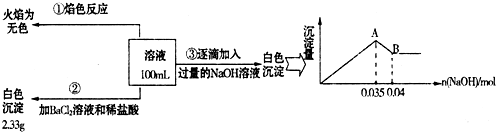
请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为 .
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为 .
③试确定NO3-是否存在? (填“存在”、“不存在”或“不确定”),若存在,试计算c(NO3-)= (若不存在,此问不必作答).
查看习题详情和答案>>
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的
(2)自来水厂常用高铁酸钠(Na2FeO4,强氧化剂)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理
(3)某无色废水中可能含有Fe2+、Al3+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图所示:

请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为
③试确定NO3-是否存在?
(2012?石家庄一模)目前高铁酸钠(Na2FeO4)被广泛应用于水处理,具有高效、无毒的优点.
(1)将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式
(2)某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和0H-未列出):
常温下,取一定量经Na2FeO4处理过的海水为原料制备精制食盐水和MgCl2?7H20,过程如下:
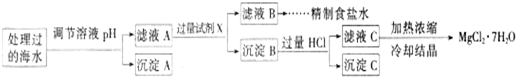
注:离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;Ksp[Fe(OH)3]=1.0×10-38 Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积变化忽略不计.
①表格中的a
②沉淀A的组成为
③加入的过量试剂X为
④加入过量HCl的作用为
查看习题详情和答案>>
(1)将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式
2
2
Fe(OH)3+3
3
ClO-+4OH-
4OH-
=2
2
FeO42-+3
3
Cl-+5H2O
5H2O
(2)某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和0H-未列出):
| 离子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |

注:离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;Ksp[Fe(OH)3]=1.0×10-38 Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积变化忽略不计.
①表格中的a
>
>
0.16 (填“<”、“>”或“=”).②沉淀A的组成为
Fe(OH)3
Fe(OH)3
(填化学式)③加入的过量试剂X为
Ba(OH)2
Ba(OH)2
(填化学式)④加入过量HCl的作用为
使Mg(OH)2全部溶解转化为MgCl2;在加热浓缩滤液C时抑制Mg2+水解
使Mg(OH)2全部溶解转化为MgCl2;在加热浓缩滤液C时抑制Mg2+水解
.目前高铁酸钠(Na2FeO4)被广泛应用于水处理,具有高效、无毒的优点.
(1)将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式
______Fe(OH)3+______ClO-+______=______FeO42-+______Cl-+______
(2)某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和0H-未列出):
| 离子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
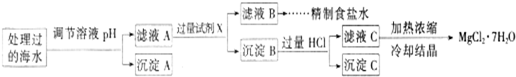
注:离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;Ksp[Fe(OH)3]=1.0×10-38 Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积变化忽略不计.
①表格中的a______0.16 (填“<”、“>”或“=”).
②沉淀A的组成为______ (填化学式)
③加入的过量试剂X为______ (填化学式)
④加入过量HCl的作用为______. 查看习题详情和答案>>
2012年3月22日是第二十届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的______倍.
(2)自来水厂常用高铁酸钠(Na2FeO4,强氧化剂)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理______.
(3)某无色废水中可能含有Fe2+、Al3+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图所示: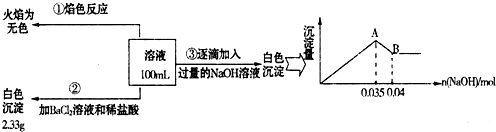
请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为______.
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为______.
③试确定NO3-是否存在?______(填“存在”、“不存在”或“不确定”),若存在,试计算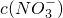 =______(若不存在,此问不必作答).
=______(若不存在,此问不必作答).
查看习题详情和答案>>
目前高铁酸钠(Na2FeO4)被广泛应用于水处理,具有高效、无毒的优点。
(1)在处理水的过程中,Na2FeO4起到杀菌、消毒、净水的作用,请说明应用了Na2FeO4的哪些性质:__________________________________________________________________________
(2) 某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和OH-未列出):
| 离子 | SO | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |
常温下,取一定量经Na2FeO4处理过的海水为原料制备精制食盐水和MgCl2·7H2O,过程如下:

Ksp[Fe(OH)3]=1.0×10-38;Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积的变化忽略不计。
① 表格中的a________0.16(填“<”、“>”或“=”)。
② 沉淀A的组成为________(填化学式);在调节溶液pH时,理论上应调节的pH的范围是________。
③ 加入的过量试剂X为____________________(填化学式)。
④ 加入过量HCl的作用为_________________________________________________。
查看习题详情和答案>>