网址:http://m.1010jiajiao.com/timu3_id_396033[举报]
 元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.
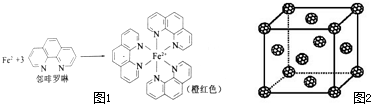
元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰.相关的反应如下:
4FeCl3+2NH2OH?HCl→4FeCl2+N2O↑+6HCl+H2O
①Fe2+在基态时,核外电子排布式
②羟胺中(NH2OH)采用SP3杂化的原子有
③Fe2+与邻啡罗啉形成的配合物中,配位数为
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3 不易与Cu2+形成配离子,其原因是
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周 期电负性最小的原子可作为容体掺入C60 晶体的空隙中,形成具有良好的超导性的掺杂C60 化合物.现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60 晶体的四面体空隙后,所形成的掺杂C60 化合物的化学式为
(10分)下表是元素周期表的一部分,表中字母分别代表某一化学元素,请回答有关问题。

(1)人们曾认为g、h、i不发生化学反应,因而把它们叫做稀有气体,但是后来发现这族气体可以参加化学反应,你认为g、h、i中最有可能首先被发现可以参加化学反应的元素是_______(写元素符号);g、h、i第一电离能由大到小的顺序为______。(用元素符号表示)
(2)e元素原子结构示意图为_____ __。d元素原子核外电子排布式为_____ __。
(3)a的阴离子半径__ __b的阳离子半径(填大于、等于、小于)。
(4)在元素周期表中有一个对角线规则,其中包括b、c的化合物的性质十分相似。则b的氯化物分别与少量和过量的氢氧化钠溶液发生反应的离子方程式分别为(要表达出具体的元素符号,下同)______ _______ __________;___________ ________________。
(5)f的+4价氧化物可与浓盐酸反应,且已知其氧化性强于氯气,则该氧化物与浓盐酸反应的化学方程式可表示为_____________ _________________________。
(6)元素周期表中第6周期中的镧系元素共有 种,它们原子的电子层结构和性质十分相似。
(7)元素k的氢化物乙可由两种10个电子的微粒组成的化合物甲(化学式X3Y2)与水剧烈反应能生成。甲与水反应的化学反应方程式为:____ ___。
查看习题详情和答案>>
(10分)下表是元素周期表的一部分,表中字母分别代表某一化学元素,请回答有关问题。
(1)人们曾认为g、h、i不发生化学反应,因而把它们叫做稀有气体,但是后来发现这族气体可以参加化学反应,你认为g、h、i中最有可能首先被发现可以参加化学反应的元素是_______(写元素符号);g、h、i第一电离能由大到小的顺序为______。(用元素符号表示)
(2)e元素原子结构示意图为_____ __。d元素原子核外电子排布式为_____ __。
(3)a的阴离子半径__ __b的阳离子半径(填大于、等于、小于)。
(4)在元素周期表中有一个对角线规则,其中包括b、c的化合物的性质十分相似。则b的氯化物分别与少量和过量的氢氧化钠溶液发生反应的离子方程式分别为(要表达出具体的元素符号,下同)______ _______ __________;___________ ________________。
(5)f的+4价氧化物可与浓盐酸反应,且已知其氧化性强于氯气,则该氧化物与浓盐酸反应的化学方程式可表示为_____________ _________________________。
(6)元素周期表中第6周期中的镧系元素共有 种,它们原子的电子层结构和性质十分相似。
(7)元素k的氢化物乙可由两种10个电子的微粒组成的化合物甲(化学式X3Y2)与水剧烈反应能生成。甲与水反应的化学反应方程式为:____ ___。
①取1 000 g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
②将待测溶液转移入250 mL锥形瓶中,并加入2—3滴0.2%的X溶液;
③用标准碘溶液滴定待测溶液至终点,消耗21.40 mL标准I2溶液,发生的反应是H3AsO3+I2+H2O——H3AsO4+I-+H+(未配平)
请回答下列问题:
(1)As位于元素周期表中第_________周期第_________族;简述对少量的中草药样品进行前期处理制得待测溶液的方法是_____________________________________。
(2)0.2% X溶液名称是_____________,滴定到终点时锥形瓶中产生的现象是_____________________________________。
(3)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.100 0 g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1 000 mL而制得,请用离子方程式说明标准碘溶液的形成:____________________________________。
(4)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过 2.000 mg/kg,试通过计算说明该中草药样品是否合格。
查看习题详情和答案>>
(2)e是周期表中的___________族,元素原子结构示意图为_______________。
(3)a的阴离子半径____________b的阳离子半径(填大于、等于、小于)。
(4)在元素周期表中有一个对角线规则,其中包括b、c的化合物的性质十分相似。则b的氯化物分别与少量和过量的氢氧化钠溶液发生反应的离子方程式分别为(要表达出具体的元素符号,下同_______________________________;________________________。
(5)f的+4价氧化物可与浓盐酸反应,且已知其氧化性强于氯气,则该氧化物与浓盐酸反应的化学方程式可表示为_________________________。
(6)元素周期表中第6周期中的镧系元素共有___________种,它们原子的电子层结构和性质十分相似。
(7)元素k的氢化物乙可由两种10个电子的微粒组成的化合物甲(化学式X3Y2)与水剧烈反应能生成。甲与水反应的化学反应方程式为:________________________。甲属于_______________晶体(类型)。工业上生产化合物乙时,既要增大乙的产量,又要提高乙的产率,可采取的措施是(填写下列合理选项的序数)_______________。
①减压 ②加压 ③升温 ④降温 ⑤适宜的温度和压强 ⑥加催化剂
⑦及时从平衡体系中分离出乙 ⑧分离出乙后的原料气循环使用并补充原料