网址:http://m.1010jiajiao.com/timu3_id_39582[举报]
(1) 化学电源能够把________能转化为________能。组成原电池的条件 之一是________插入电解质溶液中。下列属于化学电源的有_________。①蓄电池 ② 锌锰电池③充电电池④一次性电池
(2)化学电源的组成可以表示为:(一)负极材料‖A‖正极材料(+)。A表示________,
离子在A中的电阻比电子在金属中的电阻________。对于不漏电的电池电子A中 ________(填通过、不通过)。
(3)1991年Sony公司首次推出商品化的锂离子电池,此后锂离子电池,此后锂子电 池的厂家如雨后春笋般在全世界出现,锂离子电池的品种和数量也在逐年增加。锂离 子电池的电压高,单个电池的电压是3.6V。锂离子电池的正极材料是锂的过渡金属氧 化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负级材料 是可插入锂的碳材料。
①锂在元素周期表中位于第________周期,第________族。②锂离子电池所用的下负 极材料都是不污染环境的无毒无害物质,作为密封电池无毒无害,可以放心使用,属 于绿色能源。而铝镍在生产过程中污染环境。铝镍电池的有毒物质是________,它作 为电池的________级。
查看习题详情和答案>>
2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。

据此判断:
①该反应的ΔH________0(填“>”或“<”)
②在T2温度下,0~2 s内的平均反应速率v(N2)=______________________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。


(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g)??N2O4(g) ΔH2=-56.9 kJ/mol
写出CH4(g)催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式:________________________________________________________________________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的
目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为__________________________。

③常温下,0.1 mol·L-1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=________。
查看习题详情和答案>>
电池在人们的日常生活、工农业生产、教学、科研等各个方面具有广泛的应 用。电池按不同的划分标准可以划分为不同的种类,用氧化还原反应设计的电池统称 为化学电源。
(1) 化学电源能够把________能转化为________能。组成原电池的条件 之一是________插入电解质溶液中。下列属于化学电源的有_________。①蓄电池 ② 锌锰电池③充电电池④一次性电池
(2)化学电源的组成可以表示为:(一)负极材料‖A‖正极材料(+)。A表示________,
离子在A中的电阻比电子在金属中的电阻________。对于不漏电的电池电子A中 ________(填通过、不通过)。
(3)1991年Sony公司首次推出商品化的锂离子电池,此后锂离子电池,此后锂子电 池的厂家如雨后春笋般在全世界出现,锂离子电池的品种和数量也在逐年增加。锂离 子电池的电压高,单个电池的电压是3.6V。锂离子电池的正极材料是锂的过渡金属氧 化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负级材料 是可插入锂的碳材料。
①锂在元素周期表中位于第________周期,第________族。②锂离子电池所用的下负 极材料都是不污染环境的无毒无害物质,作为密封电池无毒无害,可以放心使用,属 于绿色能源。而铝镍在生产过程中污染环境。铝镍电池的有毒物质是________,它作 为电池的________级。
查看习题详情和答案>>
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。(已知:碳酸不能溶解Al(OH)3沉淀)

(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3 b.结合质子的能力:CO![]() > AlO2->HCO3-
> AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4 d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是
通过 现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是 , ;
若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg ,理论上至少需要1 molL-1 HNO3的体积为 L。
查看习题详情和答案>>
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”.其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O═2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2═2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:______.
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | ______ | ______ |
| 步骤2 | ______ | ______ |
| 步骤3 | ______ | ______ |
| 步骤4 | 洗涤 | ______ |
| 步骤5 | ______ | 得到FeSO4溶液 |
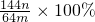 .该学生的计算是否正确:______,请说明理由______.
查看习题详情和答案>>
.该学生的计算是否正确:______,请说明理由______.
查看习题详情和答案>>