题目内容
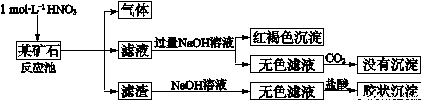
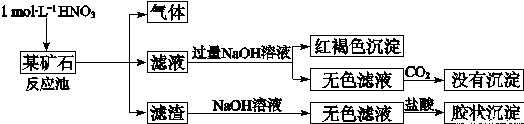
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。(已知:碳酸不能溶解Al(OH)3沉淀)

(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3 b.结合质子的能力:CO![]() > AlO2->HCO3-
> AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4 d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是
通过 现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是 , ;
若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg ,理论上至少需要1 molL-1 HNO3的体积为 L。
(1)2C+ SiO2 Si + 2CO↑ (2分) (2)ac(2分)
(3) SiO2+2OH- = SiO32-+H2O(2分) 无色溶液中通入CO2 无白色沉淀生成(1分)
(4)3FeCO3+10H++NO3- = 3Fe3+ +3CO2↑+NO↑+5H2O(2分)
(5)NO循环使用能减少环境污染; NO跟H2O、O2反应后又得到硝酸提高原料利用率 (2分)
3.33×104(2分)