网址:http://m.1010jiajiao.com/timu3_id_393692[举报]
(08上海嘉定区期末)某实验小组演绎实验室制氯化氢的方法,用溴化钠与浓硫酸作用以图甲为主要装置(固定、加热等仪器均略去)制取溴化氢气体。

(1) 甲中装在蒸馏烧瓶中的小试管的作用是__________________________________
(2) 实验开始后,发现蒸馏烧瓶中产生大量红棕色气体。我们学到过的本身为红棕色或发生反应后会变为红棕色的气体有__________________________,从本实验的反应物分析,该气体应该是______________________。
(3) 为确定从蒸馏烧瓶中排出的气体中有无溴化氢气体,设计了图乙的装置作试验,指出图乙装置中的错误a_________________________、b___________________________。
(4) 图乙装置的广口瓶和试管中分别装有的试剂可以是( )
A、氢氧化钠溶液、硝酸银溶液 B、四氯化碳、硝酸银溶液
C、硝酸银溶液、四氯化碳 D、蒸馏水、硝酸银溶液
(5) 若要在实验室制取碘化氢气体,选择的反应物是( )
A、氢气和碘 B、碘化钠和浓硫酸
C、碘化钾和浓盐酸 D、碘化钾和浓磷酸
(6)若在甲装置的蒸馏烧瓶中分别装入下列药品:a锌粉、b二氧化锰粉、c大理石粉三种固体药品,它们若能与稀盐酸反应,请写出制取气体的化学方程式_________________________________________________________________________
查看习题详情和答案>>
(08淄博市模拟)(18分)某学习兴趣小组探究废干电池(锌筒内填有炭粉、MnO2、NH4Cl等的糊状物)的回收利用,并用回收的物质进行如下实验。
I.(1)从废干电池中提取NH4Cl。
① 利用该糊状物提取NH4Cl前两步的操作为:a.溶解 b. 。
② 甲同学设想:将分离出的NH4Cl溶液蒸发、结晶、灼烧,就可以制得纯净的NH4Cl。请对甲同学的方案作出评价并说明理由:______________________________________
。
(2)制取氨气。
① 乙同学要制备并收集到纯净的氨气,下列各反应及操作中合理的是
a.将氯化铵固体加热分解 b.将浓氨水滴入氢氧化钠固体中
c.将氢氧化钠固体加入浓氨水中 d.将氯化铵浓溶液滴入氢氧化钠固体中

② 乙同学认为将集气瓶正放在桌上(如图所示),就可以收集到纯净的氨气。
你若认为可行,请说明其操作:_____________________________。
你若认为不可行,请说明其理由:___________________________。
Ⅱ.丙同学利用上面得到的氨气制取氨水并进行了如下探究实验:
(3)为探究NH3?H2O是否是弱电解质。
丙该同学设计方案如下:① 将1.12L(标况)NH3完全溶于水,配得溶液500mL;
② ;③分析数据,即
可得出结论。
请把最简单的实验步骤②,填写在上面的空格中。
 (4)探究氨水与盐酸的反应过程。
(4)探究氨水与盐酸的反应过程。
丙同学进行了如下实验:向25mL上述氨水中逐
滴滴加同浓度的盐酸,测定反应过程中溶液pH并绘
制其pH变化曲线(如图)。请回答:
①酸碱恰好完全中和时的pH点应是_________
(填A或B或D),此时溶液中c(NH3?H2O)+c(NH4+)=______mol?L-1,溶液中
各离子的浓度由大到小的顺序为 。
III.请参与探究
(5)请完成以下探究实验报告。
【探究课题】比较在25℃、0.1mol?L-1的NH3?H2O溶液和0.1mol?L-1的NH4Cl溶液中,NH3?H2O的电离程度与NH4+水解程度的相对大小。
【探究方案】 查看习题详情和答案>> (2010?定海区模拟)I.(1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
(2010?定海区模拟)I.(1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是(2)若室温下pH=2的盐酸和醋酸溶液各100mL,分别加水稀释后使pH=4,设盐酸中加入水的体积为V1,醋酸溶液中加入的水的体积为V2,则:V1
II.已知常温下,Cu(OH)2 的溶度积常数为Ksp=2×10 -20.又知常温下某CuSO4溶液里 Cu2+浓度为0.02mol?L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于
III.常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色,则该溶液呈
 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.(1)写出溶液B的溶质是
(2)参照以下框图形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作).

(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定.
①判断到达滴定终点的现象是
②某同学称取 2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用0.0050mol?L-1KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是
[实验I]硫的质量确定:
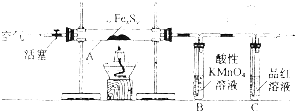
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.0g铁硫簇结构(含有部分不反应的杂质),在试管B中加入50mL 0.1mol?L-1的酸性KMnO4溶液,在试管C中加入品红溶液.通入空气并加热,发现固体逐渐转变为红棕色.待固体完全转化后将B中溶液转移至250mL容量瓶,洗涤试管B后定容.取25.00mL该溶液用0.01mol?L-1的草酸(H2C2O4)进行测定剩余KMnO4溶被浓度的滴定.记录数据如下:
| 滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
[实验Ⅱ]铁的质量确定:
将实验I硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.6g固体.
试回答下列问题:
(1)检查“实验I”中装置气密性的方法是
(2)滴定终点的判断方法是
(3)试管C中品红溶液的作用是
(4)根据实验I和实验II中的数据可确定该铁硫簇结构的化学式为
[问题探究]滴定过程中发现,细心的小明发现该KMnO4颜色褪去的速率较平常滴定时要快的多.为研究快的原因.甲同学继续进行了下列实验,实验数据如下表:
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0 (另加少量可溶于水MnSO4粉末) |
2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |