摘要:将0.2mol甲物质加入250mL 0.4mol·L-1的盐酸中.充分反应后.再加入0.1mol乙物质.在整个过程中.产生的H2在标准状况下的体积最多的是( ) A B C D 甲 K K Na Al 乙 Na Mg Al Mg
网址:http://m.1010jiajiao.com/timu3_id_393409[举报]
短周期中的A、B、C、D、E 5种元素,原子序数依次增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C2-离子与D+离子的核外电子数相等;B原子与D+离子的核外电子数之和等于E原子的核外电子数,且D、E两元素能形成微粒个数比为1:1的离子化合物.
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为
(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为
(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为
查看习题详情和答案>>
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为
次氯酸
次氯酸
.(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
;阴极区溶液的pH大于7
大于7
.(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为
Cl2+H2O2=2HCl+O2↑
Cl2+H2O2=2HCl+O2↑
.(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为
NH4Cl(或NH4NO3)
NH4Cl(或NH4NO3)
,Y的化学式为NaOH
NaOH
.②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为
c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)[或c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)]
c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)[或c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)]
.有五种摩尔质量均为44g/mol的化合物甲、乙、丙、丁、戊,均由短周期元素组成。对甲的捕获在降低温室气体排放中具有重要的作用。乙为烃,等物质的量的乙与丁充分燃烧产物为甲与水,且生成水的质量前者是后者的2倍,丙在一定条件下分解获得两种单质,两单质放电时反应生成A,A遇空气变成红棕色气体B。戊是一种极不稳定的物质,在1180℃以下不存在。科学家用质谱仪在工业制硅的反应产物中证实了其存在。
(1)丁的分子式????????????? ,甲的电子式???????????????? 。
(2)若生成戊的反应中氧化产物与还原产物为同一物质,写出生成戊的化学方程式???????? 。
(3)把铁和铜混和物放入一定量B通入水后形成的稀溶液中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液中一定含有的溶质是????????????????????????????? 。
(4)将0.2mol乙完全燃烧后生成的气体全部缓慢通入300mL某浓度的NaOH溶液中,气体完全被吸收,溶液中NaOH无剩余,则NaOH溶液的浓度为?????? (若有定值则写具体数值,无定值则写范围)。
(5)将等物质的量A、B的混合物溶于NaOH溶液中得到只含有一种溶质的溶液,此溶质的化学式为????????????? ,设计简单实验方案证明溶液中含有此溶质?????????????????????? 。
查看习题详情和答案>>
短周期中的A、B、C、D、E 5种元素,原子序数依次增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C2-离子与D+离子的核外电子数相等;B原子与D+离子的核外电子数之和等于E原子的核外电子数,且D、E两元素能形成微粒个数比为1:1的离子化合物.
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为______.
(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为______;阴极区溶液的pH______.
(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为______.
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为______,Y的化学式为______.
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为______.
查看习题详情和答案>>
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为______.
(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为______;阴极区溶液的pH______.
(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为______.
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为______,Y的化学式为______.
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为______.
查看习题详情和答案>>
短周期中的A、B、C、D、E 5种元素,原子序数依次增大,A、D同主族;A、B的原子序数之和等于C的原子序数;C2-离子与D+离子的核外电子数相等;B原子与D+离子的核外电子数之和等于E原子的核外电子数,且D、E两元素能形成微粒个数比为1:1的离子化合物.
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为______.
(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为______;阴极区溶液的pH______.
(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为______.
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为______,Y的化学式为______.
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为______.
查看习题详情和答案>>
(1)由A、C、E 三种元素组成的一种化合物常用作消毒液其名称为______.
(2)D、E元素可组成化合物甲,用石墨为电极电解甲的水溶液时,阳极的电极反应式为______;阴极区溶液的pH______.
(3)A、C元素可组成原子个数比为1:1的共价化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为______.
(4)A、B、C、D、E中的任意三种元素可组成多种化合物,X和Y是其中的两种.X和Y都是既含离子键又含共价键的离子化合物;将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的pH<7,Y水溶液的pH>7.将0.2mol?L-1的X溶液与0.1mol?L-1的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为______,Y的化学式为______.
②混合溶液中各种带电微粒的物质的量浓度由大到小的顺序为______.
氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中.某化学小组同学对含氰化物废水处理进行研究.
I.查阅资料:含氰化物的废水破坏性处理方法.
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等.
II.实验验证:破坏性处理CN-的效果.
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
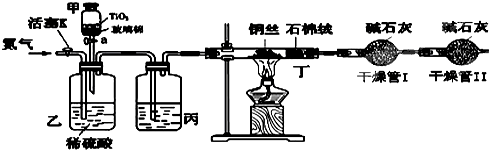
步骤1:取一定量废水进行加热蒸发、浓缩.
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol?L-1)倒入甲中,塞上橡皮塞.
步骤3:
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞.
步骤5:打开活塞K,通一段时间N2,关闭活塞K.
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式
(2)完成步骤3
(3)丙装置中的试剂是
(4)干燥管Ⅱ的作用是
(5)请简要说明实验中通入N2的目的是
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为
查看习题详情和答案>>
I.查阅资料:含氰化物的废水破坏性处理方法.
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等.
II.实验验证:破坏性处理CN-的效果.
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:

步骤1:取一定量废水进行加热蒸发、浓缩.
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol?L-1)倒入甲中,塞上橡皮塞.
步骤3:
点燃酒精灯对丁装置加热
点燃酒精灯对丁装置加热
.步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞.
步骤5:打开活塞K,通一段时间N2,关闭活塞K.
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式
2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O
2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O
.(2)完成步骤3
点燃酒精灯对丁装置加热
点燃酒精灯对丁装置加热
.(3)丙装置中的试剂是
浓硫酸
浓硫酸
,丁装置的目的是除去Cl2
除去Cl2
.(4)干燥管Ⅱ的作用是
防止空气中的水和CO2进入干燥管I中影响对CO2的测量
防止空气中的水和CO2进入干燥管I中影响对CO2的测量
.(5)请简要说明实验中通入N2的目的是
使装置中的CO2全部被排到干燥管I中被吸收,减少误差
使装置中的CO2全部被排到干燥管I中被吸收,减少误差
.(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为
80%
80%
.