摘要:3.有反应M2O7n-+S2-+H+→M3++S↓+H2O.其中氧化剂与还原剂的物质的量之比为1∶3. 则M2O7n-中M的化合价是 A.+2 B.+4 C.+6 D.+7
网址:http://m.1010jiajiao.com/timu3_id_393355[举报]
(1)今有反应2H2+O2
2H2O,构成燃料电池,则负极通的应是
(2)如把KOH改为稀H2SO4作电解质,则电极反应式为:负极:
查看习题详情和答案>>
| ||
H2
H2
,电极反应式为:H2-2e-+2OH-=2H2O
H2-2e-+2OH-=2H2O
;正极通的应是O2
O2
,电极反应式为:O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.(2)如把KOH改为稀H2SO4作电解质,则电极反应式为:负极:
H2-2e-=2H+
H2-2e-=2H+
正极:O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
.(2013?烟台模拟)硫、氮、碘都是重要的非金属元素.
(1)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O.该反应中还原剂是
(2)已知:2I(g)═I2(g)△H=-151 kJ?mol-1;2H(g)═H2(g)△H=-436 kJ?mol-1;HI(g)=H(g)+I(g)△H=+298 kJ?mol-1.相同条件下,H2与I2反应生成HI的热化学方程式为:H2(g)+I2(g)=2HI(g)△H=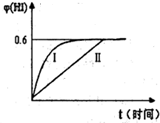
(3)将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g)?2HI(g)并达平衡.HI的体积分数φ(HI)随时间变化如图曲线II所示:
①达到平衡时,I2(g)的物质的量浓度为
②保持加入的反应物的物质的量不变,若改变反应条
件,在某一条件下φ(HI)的变化如曲线I所示,则该条件可能是
A.恒温条件下,缩小反应的容积 B.恒容条件下.加入适当催化剂
C.在恒容下,升高温度 D.在恒容下,充入N2使容器压强增大
③若保持温度不变,在另一相同的2L密闭容器中加入1mol H2(g)和2mol Hl(g),发生反应达到平衡时,H2的体积分数为
查看习题详情和答案>>
(1)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O.该反应中还原剂是
H2S
H2S
.若反应过程中转移了0.3mol电子,则反应的HNO3的质量是6.3
6.3
g.(2)已知:2I(g)═I2(g)△H=-151 kJ?mol-1;2H(g)═H2(g)△H=-436 kJ?mol-1;HI(g)=H(g)+I(g)△H=+298 kJ?mol-1.相同条件下,H2与I2反应生成HI的热化学方程式为:H2(g)+I2(g)=2HI(g)△H=
-9
-9
kJ?mol-1.
(3)将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g)?2HI(g)并达平衡.HI的体积分数φ(HI)随时间变化如图曲线II所示:
①达到平衡时,I2(g)的物质的量浓度为
0.05
0.05
mol?L-1.②保持加入的反应物的物质的量不变,若改变反应条
件,在某一条件下φ(HI)的变化如曲线I所示,则该条件可能是
AB
AB
(填编号),在这种条件下平衡常数K值不变
不变
(填“增大”、“变小”或“不变’,).A.恒温条件下,缩小反应的容积 B.恒容条件下.加入适当催化剂
C.在恒容下,升高温度 D.在恒容下,充入N2使容器压强增大
③若保持温度不变,在另一相同的2L密闭容器中加入1mol H2(g)和2mol Hl(g),发生反应达到平衡时,H2的体积分数为
37%
37%
.某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.
已知该反应中H2O2只发生如下过程:H2O2-→O2.
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O =2Cr(OH)3↓+3O2↑+2H2O.
=2Cr(OH)3↓+3O2↑+2H2O.
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
查看习题详情和答案>>
已知该反应中H2O2只发生如下过程:H2O2-→O2.
(1)该反应中的还原剂是
H2O2
H2O2
.(2)该反应中,发生还原反应的过程是
H2CrO4
H2CrO4
→Cr(OH)3
Cr(OH)3
.(3)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目
 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
3.36 L
3.36 L
.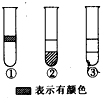 向盛有溴水的三支试管中分别加入苯、四氯化碳和1--己烯(若有反应发生,则溴能反应完全),振荡后静置,出现如图所示现象.则加入的试剂分别是( )
向盛有溴水的三支试管中分别加入苯、四氯化碳和1--己烯(若有反应发生,则溴能反应完全),振荡后静置,出现如图所示现象.则加入的试剂分别是( )| A、①是CCl4,②是苯,③是1-己烯 | B、①是1-己烯,②是CCl4,③是苯 | C、①是苯,②是 CC14,③是1-己烯 | D、①是苯,②是1-己烯,③是CC4 |
Ⅰ.过氧化氢(H2O2)的水溶液俗称双氧水,近年来倍受人们的青睐,被称为“绿色氧化剂”.
(1)写出H2O2的电子式
 ,其分子内存在
,其分子内存在
(2)你认为H2O2被成为“绿色氧化剂”的主要原因是
(3)与H2O2分子具有相同电子数的双原子单质分子为(写化学式)
(4)某工业废水中含有一定量氯气,为了除去氯气,常加入H2O2作脱氯剂,写出该反应的化学方程式为
(5)将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为
(6)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里:
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应的化学方程式为
(2)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
查看习题详情和答案>>
(1)写出H2O2的电子式


极性键
极性键
键和非极性
非极性
键.(2)你认为H2O2被成为“绿色氧化剂”的主要原因是
还原产物为水,对环境无污染
还原产物为水,对环境无污染
.(3)与H2O2分子具有相同电子数的双原子单质分子为(写化学式)
F2
F2
,与H2O2分子具有相同电子数的三原子化合物分子为(写化学式)H2S
H2S
.(4)某工业废水中含有一定量氯气,为了除去氯气,常加入H2O2作脱氯剂,写出该反应的化学方程式为
Cl2+H2O2=2HCl+O2↑
Cl2+H2O2=2HCl+O2↑
,反应中H2O2作还原
还原
剂.(5)将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
,反应中H2O2作氧化剂
氧化剂
剂.(6)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里:
2
2
MnO4-+5
5
H2O2+6
6
H+═2
2
Mn2++8
8
H2O+5O2↑
5O2↑
.Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应的化学方程式为
3H2O2+2H2CrO4=3O2↑+2Cr(OH)3+2H2O
3H2O2+2H2CrO4=3O2↑+2Cr(OH)3+2H2O
.(2)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
3.36L
3.36L
.