摘要:13.下列物质:1Cl22Na 3Na2O2 4NO2分别与水反应.氧化剂与还原剂的物质的量之比为1:1的是 A. 12 B.23 C.123 D.1234
网址:http://m.1010jiajiao.com/timu3_id_386090[举报]
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4
HBr+NaHSO4 ①
R-OH+HBr
R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下;
请回答下列问题:
(1)溴代烃的水溶性
(2)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在
(3)制备操作中,加入的浓硫酸必需进行稀释,起目的是
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于
查看习题详情和答案>>
NaBr+H2SO4
| ||
R-OH+HBr
| 加热 |
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g?cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)溴代烃的水溶性
小于
小于
醇 (填“大于”、“等于”或“小于”);其原因是醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键
醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键
.(2)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在
下层
下层
(填“上层”、“下层”或“不分层”).(3)制备操作中,加入的浓硫酸必需进行稀释,起目的是
abc
abc
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
c
c
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于
平衡向生成溴乙烷的方向移动(或反应②向右移动)
平衡向生成溴乙烷的方向移动(或反应②向右移动)
;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷和正丁醇的沸点相差不大
1-溴丁烷和正丁醇的沸点相差不大
.下列物质与其用途完全符合的有( )
①Na2CO3-制玻璃 ②SiO2-太阳能电池 ③AgI-人工降雨 ④NaCl-制纯碱⑤Al2O3-焊接钢轨 ⑥NaClO-消毒剂 ⑦Fe2O3-红色油漆或涂料 ⑧MgO-耐火材料.
①Na2CO3-制玻璃 ②SiO2-太阳能电池 ③AgI-人工降雨 ④NaCl-制纯碱⑤Al2O3-焊接钢轨 ⑥NaClO-消毒剂 ⑦Fe2O3-红色油漆或涂料 ⑧MgO-耐火材料.
查看习题详情和答案>>
在实验室里可用图一所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
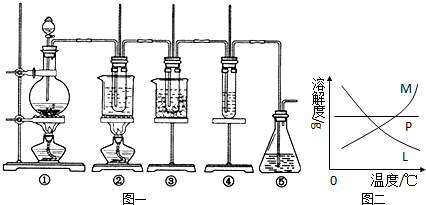
图一中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.请填写下列空白:
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
(4)反应完毕经冷却后,②的试管中有大量晶体析出.图二中符合该晶体溶解度曲线的是
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
(6)一定量的氢气在氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液(密度为1.2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol.所得溶液中Cl-离子的物质的量
查看习题详情和答案>>

图一中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.请填写下列空白:
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A、C
A、C
(已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>FeCl3).A.NaBiO3 B.FeCl3 C.PbO2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
制取温度不同
制取温度不同
; ②制取时碱的浓度也不同
制取时碱的浓度也不同
.(4)反应完毕经冷却后,②的试管中有大量晶体析出.图二中符合该晶体溶解度曲线的是
M
M
(填写编号字母);从②的试管中分离出该晶体的方法是过滤
过滤
(填写实验操作名称).(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
否
否
.为什么?石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
.(6)一定量的氢气在氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液(密度为1.2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol.所得溶液中Cl-离子的物质的量
0.250mol
0.250mol
.工业上以乙烯为原料,合成化学式为C3H6O3的化合物.
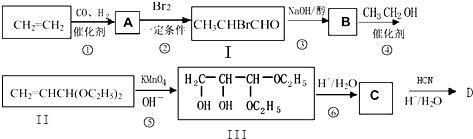
已知:
请回答相关的问题:
(1)写出下列物质的结构简式:A:
(2)写出反应③的化学方程式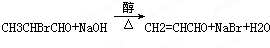
 .
.
(3)D在浓硫酸存在条件下加热,可生成五原子环状化合物E(C4H6O4),请写出反应的化学方程式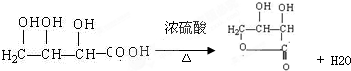
 .
.
(4)下列说法正确的是
A.化合物Ⅱ的分子式C5H9O2
B.反应④的目的是防止-CHO在第⑤步被氧化
C.反应③是消去反应,反应④是酯化反应
D.化合物D可以发生缩聚反应得到高分子化合物
(5)化合物F与C互为同分异构体,且化合物F满足以下条件:
①取等物质的量F分别与NaHCO3、Na充分反应产生CO2和H2比为1:1
②化合物F符合下面的核磁共振氢谱图 ,化合物F的结构简式为
,化合物F的结构简式为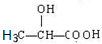
 .
.
查看习题详情和答案>>

已知:

请回答相关的问题:
(1)写出下列物质的结构简式:A:
CH3CH2CHO
CH3CH2CHO
;C:HOCH2CH(OH)CHO
HOCH2CH(OH)CHO
(2)写出反应③的化学方程式


(3)D在浓硫酸存在条件下加热,可生成五原子环状化合物E(C4H6O4),请写出反应的化学方程式


(4)下列说法正确的是
BD
BD
A.化合物Ⅱ的分子式C5H9O2
B.反应④的目的是防止-CHO在第⑤步被氧化
C.反应③是消去反应,反应④是酯化反应
D.化合物D可以发生缩聚反应得到高分子化合物
(5)化合物F与C互为同分异构体,且化合物F满足以下条件:
①取等物质的量F分别与NaHCO3、Na充分反应产生CO2和H2比为1:1
②化合物F符合下面的核磁共振氢谱图
 ,化合物F的结构简式为
,化合物F的结构简式为
