摘要: 已知A为常见金属.X.Y为常见非金属.X.E.F.G常温下为气体.C为液体.B是一种盐.受热易分解.在工农业生产中用途较广(如被用作某些电池的电解质).现用A与石墨作电极.B的浓溶液作电解质.构成原电池.有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物已略去) 请填写下列空白: (1)反应④为A在某种气体中燃烧.生成单质Y和A的氧化物.其反应方程式为 . (2)反应②的化学方程式为 (3)反应⑤的化学方程式为 (4)原电池反应①中正极的电极反应式为 (5)B溶液在工业上常被用作焊接时的除锈剂.其应用原理是 .
网址:http://m.1010jiajiao.com/timu3_id_377194[举报]
有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复) 提示:CH3COONH4溶液为中性
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象.
(1)A是
(2)用离子方程式表示A的水溶液显碱性的原因
(3)25℃时,0.1mol?L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3?H2O)=
(4)在一定体积0.005mol?L-1的C溶液中,加入一定体积的0.00125mol?L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是
查看习题详情和答案>>
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象.
(1)A是
CH3COONa
CH3COONa
,B是NH4Cl
NH4Cl
,C是Ba(OH)2
Ba(OH)2
,D是Na2SO4
Na2SO4
.(2)用离子方程式表示A的水溶液显碱性的原因
CH3COO-+H2O?CH3COOH+OH-
CH3COO-+H2O?CH3COOH+OH-
.(3)25℃时,0.1mol?L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3?H2O)=
1×10(a-14)
1×10(a-14)
(用含a的关系式表示).c(NH4+)+c(NH3?H2O)=0.1
0.1
mol/L(填具体数值)(4)在一定体积0.005mol?L-1的C溶液中,加入一定体积的0.00125mol?L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是
1:4
1:4
. 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)?2SO3(g)△H<0
(1)该反应450℃时的平衡常数
大于
大于
500℃时的平衡常数(填“大于”、“小于”或“等于”).(2)该化学达到平衡的标志是
b、d
b、d
.a.v(O2)正=2v( SO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)恒温、密闭容器体系中充入一定量SO2、O2,反应达平衡时,某物理量随体系总压强(p)的关系如图所示所示.该物理量可能是
b、d
b、d
.a.平衡体系中SO2的体积分数
b.气体的平均相对分子质量
c.混合气体的密度
d.平衡体系中SO2的转化率
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=
0.036
0.036
mol?L-1?min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡向正反应方向
向正反应方向
移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36
0.36
mol<n(SO3)<0.40
0.40
mol.(5)压强及温度对SO2转化率的影响如表(原料气各成分的体积分数为:SO27%;O21l%;N2 82%);
| 压强转化率温度 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
400℃~500℃
400℃~500℃
℃,压强0.1
0.1
MPa.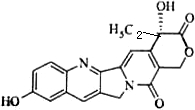 (2009?江苏)具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的说法正确的是( )
(2009?江苏)具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的说法正确的是( )