网址:http://m.1010jiajiao.com/timu3_id_375812[举报]
(1)这些有机物中,相对分子质量最小的化合物的分子式是_________________________。
(2)某两种碳原子数相同的上述有机物,若它们的相对分子质量分别为a和b,则|b-a|必定是____________(填入一个数字)的整数倍。
(3)在这些有机物中有一种化合物,它含有两个羧基。取0.262
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质。
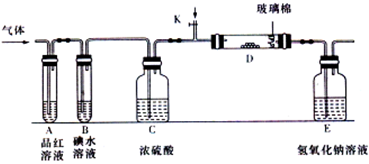
_____________;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W3完全反应后,转移
5.0×10-5mol电子,该反应的化学方程式为________________。
(2)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量的下列溶液就有沉淀生成 _________(填字母)。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(3)若由元素Y和X组成负二价酸根Z,Z中Y和X的质量比为m(Y):m(X)=4:3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生,该反应的离子方程式为____________________。
某混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1 mol水蒸气放热569.1 kJ.则该反应的热化学方程式为________.
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:
 H2+2NiOOH
H2+2NiOOH根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将________(填“增大”、“不变”或“减小”),该电极的电极反应式为________.
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+1/2O2(g)![]() CO2(g).
CO2(g).
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.

②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5 mol·L-1和1.0×10-4mol·L-1.若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4 mol·L-1,则最终尾气中CO的浓度为________mol·L-1.
(4)汽车尾气中的NOx是另一种大气污染物,可用NH3在催化剂存在下净化,写出该反应的化学方程式________.当参加反应的NH3在标准状况下体积为a L时,还原产物的质量为________g
II.图B折线c可以表达出第
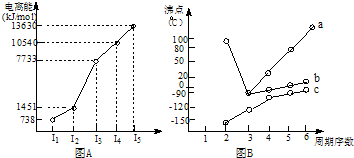
两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 | 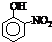 |
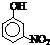 |
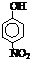 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
(2)COCl2俗称光气,分子中C原子采取
a.2个σ键 b.2个π键 c.1个σ键、1个π键.
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为
II.已知Ti3+可形成配位数为6的配合物.现有紫色和绿色两种含钛晶体,其组成均为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现:其沉淀质量:绿色晶体为紫色晶体的
| 2 |
| 3 |
(1)比较X、Y、Z的原子半径大小
(2)W与Z形成的单质分别为甲、乙,最简单氢化物分别为丙、丁,下列判断正确的是
a.稳定性:甲>乙,沸点:丙>丁 b.活泼性:甲>乙,沸点:丁>丙
c.稳定性:丙<丁,沸点:甲<乙 d.稳定性:丙>丁,沸点:甲>乙
(3)研究表明:VX2在一定条件下可被还原为晶莹透明的晶体M,其结构中原子的排列为正四面体,请写出M及其2种同素异形体的名称
(4)工业上,将Al2O3、V单质、W单质按物质的量之比1:3:1在高温下反应可制得一种无机非金属材料AlW,该反应的化学方程式为
(5)新型纳米材料ZnFe2Xa可由化合物ZnFe2X4经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示:
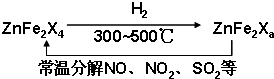
若2mol ZnFe2X a与SO2反应可生成0.75mol S,a=
(6)在t℃时,将a g NH3完全溶于X的常见氢化物,得到V mL溶液,假如该溶液的密度为d g/cm3,质量分数为w,其中含NH4+的物质的量为b mol.下列叙述正确的是
A.溶质的质量分数为w=
| a |
| Vd-a |
B.氨水的物质的量浓度为
| 1000a |
| 35V |
C.溶液中c(OH-)=
| 1000b |
| V |
D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w.