网址:http://m.1010jiajiao.com/timu3_id_375810[举报]
①Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-25kJ/mol
②3Fe2O3(s)+CO(g)?2Fe3O4(s)+CO2(g)△H=-47kJ/mol
③Fe3O4(s)+CO(g)?3FeO(s)+CO2(g)△H=+19kJ/mol
(1)试计算反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=
(2)已知1092℃时(1)中反应的平衡常数为0.35,在1L的密闭容器中,投入7.2gFeO和0.1mol CO加热到1092℃并保持该温度,反应在t1时达平衡.
①t1时反应达平衡后,CO气体的体积分数为

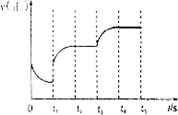
②该反应的正反应速率随时间变化情况如图甲所示,在t1时改变了某种条件,反应在t2时达平衡,改变的条件可能是
a.升高温度 b.增大CO的浓度
c.使用催化剂 d.增大压强
③如果在t3时再增加CO2的量,t4时反应又处于新平衡状态,请在甲图上画出t3~t5时间段的v(正)变化曲线

(3)炼钢尾气净化后,可直接作熔融碳酸盐燃料电池(工作原理如图乙)的燃料.则负极的电扱反应为
(4)转炉炼钢,尾气中CO体积分数达58%-70%,某钢厂先用NaOH吸收CO生成甲酸钠,再吸收SO2生成保险粉(Na2S2O4),试写出甲酸钠和氢氧化钠混合溶液与SO2生成保险粉同时生成二氧化碳的离子方程式
(5)目前我国大多数企业是将CO与水蒸气反应转换为H2,然后用H2与N2反应合成氨,若收集到标准状况下3360m3尾气,其中CO体积分数为60%,由于循环操作,假定各步转化率均为100%,理论上可获得NH3
【化学—选修5:物质结构与性质】(15分)
现有A、B、C、D、E原子序数依次增大的五种元素,它们位于元素周期表的前四周期。A元素原子的价层电子总数是内层电子总数的2倍;C元素原子的L电子层中只有两对成对电子;D元素与E元素在同周期相邻的族,它们的原子序数相差3,且D元素的基态原子有4个未成对电子。请回答下列问题:
⑴A、B、C三种元素的名称分别为 、 、 。
⑵用元素符号表示A、B、C三种元素的第一电离能由低到高的排序为 。
⑶E元素基态原子的核外电子排布式为 。
⑷A元素与氢元素能形成种类繁多的化合物,其中只含sp3杂化且相对分子质量最小的分子的VSEPR空间构型为 ;其中只含sp2杂化且相对分子质量最小的化合物的结构式为 ;其中同时含sp杂化、SP2杂化、sp3杂化且相对分子质量最小的化合物的化学式为 。
⑸A元素的一种单质的晶体结构如图甲所示,D元素的一种单质的晶体结构如图乙所示。

图甲中A原子的配位数与图乙中D原子的配位数之比为 。
(A)“物质结构与性质”课程模块
下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于ds区的元素是___________ (填编号)。
(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是________;③和⑦形成的常见化合物的化学键类型是___________。
(3)元素⑧的外围电子排布式为___________,该元素原子中未成对电子数为___________。
(4)在周期表中位于对角线的元素的性质也有一定的相似性。试写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_________________________________________________。
(5)在1 183 K以下,元素⑨形成如图甲所示基本结构单元的晶体;1 183 K以上,转变为图乙所示基本结构单元的晶体。

在1 183 K以下的晶体中,与元素⑨的原子等距离且最近的原子数为___________;在1 183 K以上的晶体中,与元素⑨原子等距离且最近的原子数为___________。
(B)“实验化学”课程模块
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为:

氧化型(蓝色)+ne-![]() 还原型(无色)。
还原型(无色)。
奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图甲。
某校化学兴趣小组用图甲装置进行下述实验:
①在250 mL锥形瓶中,依次加入
②塞紧橡皮塞,关闭活塞a、b,静置,溶液变为无色;
③打开活塞、振荡,溶液又变为蓝色;
④关闭活塞、静置,溶液又变为无色;
⑤以上步骤③④可重复多次。
请回答下列问题:
(1)若塞紧图甲中锥形瓶塞,并打开导管活塞a、b,从___________(填“左”或“右”)导管口通入足量氦气后,再关闭活塞a、b并振荡,溶液__________(填“能”或“不能”)由无色变为蓝色。
(2)如图乙所示:某学生将起初配得的蓝色溶液分装在A、B两支试管中,A试管充满溶液,B中有少量溶液,塞上橡皮塞静置片刻,两溶液均显无色。若再同时振荡A、B试管,溶液显蓝色的是___________试管。
(3)上述转化过程中葡萄糖的作用是_______________,亚甲基蓝的作用是______________。
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为______________。
(5)该实验中③④操作___________(填“能”或“不能”)无限次重复进行,理由是____________。
查看习题详情和答案>>【化学—选修5:物质结构与性质】(15分)
现有A、B、C、D、E原子序数依次增大的五种元素,它们位于元素周期表的前四周期。A元素原子的价层电子总数是内层电子总数的2倍;C元素原子的L电子层中只有两对成对电子;D元素与E元素在同周期相邻的族,它们的原子序数相差3,且D元素的基态原子有4个未成对电子。请回答下列问题:
⑴A、B、C三种元素的名称分别为 、 、 。
⑵用元素符号表示A、B、C三种元素的第一电离能由低到高的排序为 。
⑶E元素基态原子的核外电子排布式为 。
⑷A元素与氢元素能形成种类繁多的化合物,其中只含sp3杂化且相对分子质量最小的分子的VSEPR空间构型为 ;其中只含sp2杂化且相对分子质量最小的化合物的结构式为 ;其中同时含sp杂化、SP2杂化、sp3杂化且相对分子质量最小的化合物的化学式为 。
⑸A元素的一种单质的晶体结构如图甲所示,D元素的一种单质的晶体结构如图乙所示。


图甲中A原子的配位数与图乙中D原子的配位数之比为 。
查看习题详情和答案>>


(2)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如上表所示,其中A的晶体类型是___,A 的电子式为___,C的化学式为____。
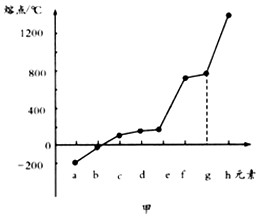
(3)第三周期元素单质的熔点变化如图甲所示,则h的元素名称是____,工业上生产h单质的化学方程式为
________________________
(4)分子甲和离子乙都含有10个电子,且离子乙的立体结构如图乙所示。写出甲、乙反应的离子方程式
________________ 。请再写出一种由短周期元素组成的、结构如图乙的分子的化学式________。