摘要:(1)①溶于水.过滤. ②在此条件下Fe3+被沉淀并保证Cu2+不被沉淀. ③小心蒸发浓缩后.冷却结晶. 加热温度不会超过100℃.加热温度改变较缓慢 (2)①CuO对H2O2的分解反应有催化作用.②盛满水的洗气瓶.量筒.导气管.
网址:http://m.1010jiajiao.com/timu3_id_375646[举报]
牙膏中的摩擦剂约占牙膏成分的50%,主要用于增强牙膏的摩擦作用和去污效果,牙膏摩擦剂一般由CaCO3、Al(OH)3或SiO2组成.某化学兴趣小组对几种品牌牙膏中摩擦剂成分及其含量进行以下探究:
(1)根据上述信息,推测摩擦剂应具备的性质有 (填序号)
①易溶于水 ②难溶于水 ③坚硬 ④柔软 ⑤颗粒较大 ⑥颗粒较小
(2)已知A品牌牙膏中的摩擦剂是Al(OH)3,取适量牙膏样品,加水成分搅拌、过滤.
①往滤渣中加入过量NaOH溶液,过滤,Al(OH)3与NaOH溶液反应的离子方程式是 .
②往①所得滤液中先通入过量CO2,再加入过量稀盐酸,观察到的现象是 .
(3)已知B品牌牙膏中的可能含有一种或两种物质,将此牙膏中的摩擦剂溶于盐酸时,发现有不溶性物质,
①对B品牌牙膏摩擦剂的成分提出合理假设:
假设1:牙膏摩擦剂的成分为SiO2
假设2:牙膏摩擦剂的成分为SiO2和CaCO3
假设3:牙膏摩擦剂的成分为 .
②设计方案对B品牌牙膏摩擦剂的成分进行实验,验证假设.请写出实验步骤以及预期现象和结论(可不填满).
限选试剂:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水
(4)已知C品牌牙膏中的摩擦剂为CaCO3,通过下列实验确定CaCO3的质量分数.取20.0g牙膏样品溶于水后过滤,将所得沉淀溶解于100mL1mol/L的盐酸中,然后从所得的溶液中取20.00mL放入锥形瓶中,用1mol/L NaOH溶液进行滴定,测得消耗的NaOH溶液体积为5.00mL,则20.0g牙膏样品消耗的盐酸为 mol,C品牌牙膏中CaCO3的质量分数为 .
查看习题详情和答案>>
(1)根据上述信息,推测摩擦剂应具备的性质有
①易溶于水 ②难溶于水 ③坚硬 ④柔软 ⑤颗粒较大 ⑥颗粒较小
(2)已知A品牌牙膏中的摩擦剂是Al(OH)3,取适量牙膏样品,加水成分搅拌、过滤.
①往滤渣中加入过量NaOH溶液,过滤,Al(OH)3与NaOH溶液反应的离子方程式是
②往①所得滤液中先通入过量CO2,再加入过量稀盐酸,观察到的现象是
(3)已知B品牌牙膏中的可能含有一种或两种物质,将此牙膏中的摩擦剂溶于盐酸时,发现有不溶性物质,
①对B品牌牙膏摩擦剂的成分提出合理假设:
假设1:牙膏摩擦剂的成分为SiO2
假设2:牙膏摩擦剂的成分为SiO2和CaCO3
假设3:牙膏摩擦剂的成分为
②设计方案对B品牌牙膏摩擦剂的成分进行实验,验证假设.请写出实验步骤以及预期现象和结论(可不填满).
限选试剂:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水成分搅拌、过滤,得滤液A和沉淀B. | / |
| 步骤2: |
|
| 步骤3: |
“阳光”牌小包装“脱氧剂”成份为Fe粉、活性炭及少量NaCl、水.某校化学兴趣小组欲探究该“脱氧剂”中Fe粉和活性炭质量之比,设计并进行了如下探究过程,请你参与实验并回答有关问题.
步骤(1)取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末.由此得出的结论为上述“脱氧剂”中的铁已部分被
步骤(2)将步骤(1)中的固体溶于水,过滤,将滤渣洗涤、干燥.该步骤的目的是
步骤(3)取步骤(2)中的滤渣,将其分为两等份,每一份质量为8.0g.将其中一份在氧气流中充分灼烧,生成的气体全部通入足量得澄清石灰水,得到干燥、纯净的沉淀20.0 g.8.0 g滤渣中活性炭的质量为
步骤(4)将步骤(3)中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全.请写出有氢气生成的化学反应方程式
步骤(5)向步骤(4)中的混合物中加入过量的氢氧化钠溶液,过滤得到的固体经洗涤后转移到坩埚中充分加热、灼烧,冷却、称量,得到6.4gFe2O3固体.
结论:该“脱氧剂”中的Fe粉和活性炭质量之比为
查看习题详情和答案>>
步骤(1)取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末.由此得出的结论为上述“脱氧剂”中的铁已部分被
氧化
氧化
;步骤(2)将步骤(1)中的固体溶于水,过滤,将滤渣洗涤、干燥.该步骤的目的是
除去NaCl
除去NaCl
;步骤(3)取步骤(2)中的滤渣,将其分为两等份,每一份质量为8.0g.将其中一份在氧气流中充分灼烧,生成的气体全部通入足量得澄清石灰水,得到干燥、纯净的沉淀20.0 g.8.0 g滤渣中活性炭的质量为
2.4g
2.4g
;步骤(4)将步骤(3)中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全.请写出有氢气生成的化学反应方程式
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
;步骤(5)向步骤(4)中的混合物中加入过量的氢氧化钠溶液,过滤得到的固体经洗涤后转移到坩埚中充分加热、灼烧,冷却、称量,得到6.4gFe2O3固体.
结论:该“脱氧剂”中的Fe粉和活性炭质量之比为
28:15
28:15
.
天宫一号(Tiangong-1)是中国第一个目标飞行器,于2011年9月29日21时16分3秒在酒泉卫星发射中心发射,它的发射标志着中国迈入中国航天“三步走”战略的第二步.天宫一号是由长征二号大推力火箭发射升空的,火箭推进剂是成功发射火箭的重要因素,推进剂的发展经历了一个漫长的过程.
(1)20世纪前,黑火药是世界上唯一的火箭用推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为2KNO3+S+3C═K2S+N2↑+3CO2↑.
①写出K2S的电子式: ;
②某化学兴趣小组进行了如下实验:
实验一:取适量黑火药溶于水,过滤,将滤液蒸发浓缩,冷却后慢慢加入浓硫酸,将混合液置于试管中并放入铜片,产生大量红棕色气体,写出该反应的离子方程式: ;
实验二:取黑火药爆炸后的残留固体,加水溶解过滤,取滤液向其中滴加新制氯水至过量,一开始溶液变浑浊后又变澄清.请设计实验方案证明该澄清溶液中含有Cl-: ;
(2)1947年,研制出第二代聚硫橡胶、高氯酸铵、铝粉复合推进剂.高氯酸铵受撞击会引发剧烈爆炸,其爆炸产物有4种,2种产物是空气中的主要成分,另一种气体产物能使湿润的蓝色石蕊试纸变红,写出该反应的化学方程式: ;
(3)20世纪60年代,美国大推力火箭使用的是液体推进剂,常用的氧化剂有双氧水、四氧化二氮、液氧;可燃物有肼(N2H4)、一甲肼、偏二甲肼、液氢等.火箭发射时将两种液体分别注入火箭发动机的燃烧室中燃烧.偏二甲肼的系统命名为1,1-二甲基联氨,它的结构简式为 ;
(4)以上的火箭推进剂一般都含有氮元素,含氮化合物种类丰富,科学家从化肥厂生产的硫酸铵中检出组成为N4H4(SO4)2的物质,该物质为易溶于水的强电解质,遇烧碱会生成N4气体,该反应的离子方程式: ;另一含氮化合物N4H4也是易溶于水的强电解质,和烧碱反应生成能使湿润的红色石蕊试纸变蓝的气体,而与盐酸反应生成的产物之一具有极强烈的爆炸性,写出该产物爆炸的化学反应方程式: .
查看习题详情和答案>>
(1)20世纪前,黑火药是世界上唯一的火箭用推进剂,黑火药是由硝酸钾、硫磺、木炭组成,黑火药爆炸的化学方程式为2KNO3+S+3C═K2S+N2↑+3CO2↑.
①写出K2S的电子式:
②某化学兴趣小组进行了如下实验:
实验一:取适量黑火药溶于水,过滤,将滤液蒸发浓缩,冷却后慢慢加入浓硫酸,将混合液置于试管中并放入铜片,产生大量红棕色气体,写出该反应的离子方程式:
实验二:取黑火药爆炸后的残留固体,加水溶解过滤,取滤液向其中滴加新制氯水至过量,一开始溶液变浑浊后又变澄清.请设计实验方案证明该澄清溶液中含有Cl-:
(2)1947年,研制出第二代聚硫橡胶、高氯酸铵、铝粉复合推进剂.高氯酸铵受撞击会引发剧烈爆炸,其爆炸产物有4种,2种产物是空气中的主要成分,另一种气体产物能使湿润的蓝色石蕊试纸变红,写出该反应的化学方程式:
(3)20世纪60年代,美国大推力火箭使用的是液体推进剂,常用的氧化剂有双氧水、四氧化二氮、液氧;可燃物有肼(N2H4)、一甲肼、偏二甲肼、液氢等.火箭发射时将两种液体分别注入火箭发动机的燃烧室中燃烧.偏二甲肼的系统命名为1,1-二甲基联氨,它的结构简式为
(4)以上的火箭推进剂一般都含有氮元素,含氮化合物种类丰富,科学家从化肥厂生产的硫酸铵中检出组成为N4H4(SO4)2的物质,该物质为易溶于水的强电解质,遇烧碱会生成N4气体,该反应的离子方程式:
化学学习小组为测定“阳光”牌小包装中Fe粉和活性炭质量之比进行了以下探究:
查阅资料:“阳光”牌小包装“脱氧剂”成份为Fe粉、活性炭及少量NaCl、水.
实验步骤:
步骤一:取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末.
步骤二:将步骤一中的固体溶于水,过滤,将滤渣洗涤、干燥,以除去“脱氧剂”中NaCl和水;
步骤三:取步骤二中的滤渣,将其分为两等份,每一份质量为16.0g.将其中一份在氧气流中充分灼烧,生成的气体全部通入足量得澄清石灰水,得到干燥、纯净的沉淀20.0 g.
步骤四:将步骤三中的另一份滤渣放入烧杯中,加入一定体积足量的稀H2SO4,微热至反应完全.
步骤五:向步骤四的混合物中加入过量的氢氧化钠溶液,过滤后得固体,经洗涤后转移到坩埚中充分加热,冷却、称量,得到固体质量仍为16g.
请回答下列问题:
(1)由步骤一可知,上述“脱氧剂”中的红棕色物质为
(2)由步骤三可知,16.0 g滤渣中活性炭的质量为
(3)综上实验所知:该“脱氧剂”中未被氧化的Fe粉和活性炭质量之比为
(4)该“脱氧剂”中,铁已被氧化的百分率为
查看习题详情和答案>>
查阅资料:“阳光”牌小包装“脱氧剂”成份为Fe粉、活性炭及少量NaCl、水.
实验步骤:
步骤一:取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末.
步骤二:将步骤一中的固体溶于水,过滤,将滤渣洗涤、干燥,以除去“脱氧剂”中NaCl和水;
步骤三:取步骤二中的滤渣,将其分为两等份,每一份质量为16.0g.将其中一份在氧气流中充分灼烧,生成的气体全部通入足量得澄清石灰水,得到干燥、纯净的沉淀20.0 g.
步骤四:将步骤三中的另一份滤渣放入烧杯中,加入一定体积足量的稀H2SO4,微热至反应完全.
步骤五:向步骤四的混合物中加入过量的氢氧化钠溶液,过滤后得固体,经洗涤后转移到坩埚中充分加热,冷却、称量,得到固体质量仍为16g.
请回答下列问题:
(1)由步骤一可知,上述“脱氧剂”中的红棕色物质为
Fe2O3
Fe2O3
(填化学式);(2)由步骤三可知,16.0 g滤渣中活性炭的质量为
2.4
2.4
g;(3)综上实验所知:该“脱氧剂”中未被氧化的Fe粉和活性炭质量之比为
7:3
7:3
;(4)该“脱氧剂”中,铁已被氧化的百分率为
50%
50%
.(2013?广州三模)根据Mg与CO2的反应推测,Na也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种.某兴趣小组用如下装置开实验探究.
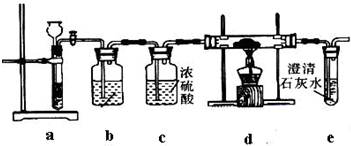
实验I:操作步骤为:
①按图连接装置,检验装置气密性,并往各装置中加入试剂;
②打开装置a上活塞一段时间;
③点燃d处酒精灯,使CO2与Na充分反应.停止加热,继续通气体使双通管冷却.
(1)装置b中装有
(2)步骤②中,当观察到
实验Ⅱ:探究反应产物及反应机理.取反应后双通管中固体物质29.2g进行如下实验:
①将固体溶于足量的水并过滤、洗涤,得到1.8g滤渣(干燥);
②将滤液加水稀释配成250mL的溶液;
③取25.00ml步骤②的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,
称量得固体质量为3.94g.
④另取25.00mL步骤②的溶液,滴加甲基橙作为指示剂,用3.0mol?L-1盐酸滴定,消耗盐酸体积为20.00mL.
(3)步骤②中固体溶于水后过滤,不溶物必须经过洗涤,洗涤的具体操作是
(4)通过实验数据分析29.2g残留固体中,含有哪几种固体?
(5)该探究条件下,钠与二氧化碳反应的化学方程式为
查看习题详情和答案>>

实验I:操作步骤为:
①按图连接装置,检验装置气密性,并往各装置中加入试剂;
②打开装置a上活塞一段时间;
③点燃d处酒精灯,使CO2与Na充分反应.停止加热,继续通气体使双通管冷却.
(1)装置b中装有
饱和NaHCO3
饱和NaHCO3
溶液.(2)步骤②中,当观察到
e装置中产生白色沉淀
e装置中产生白色沉淀
时,才能进入步骤③.实验Ⅱ:探究反应产物及反应机理.取反应后双通管中固体物质29.2g进行如下实验:
①将固体溶于足量的水并过滤、洗涤,得到1.8g滤渣(干燥);
②将滤液加水稀释配成250mL的溶液;
③取25.00ml步骤②的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,
称量得固体质量为3.94g.
④另取25.00mL步骤②的溶液,滴加甲基橙作为指示剂,用3.0mol?L-1盐酸滴定,消耗盐酸体积为20.00mL.
(3)步骤②中固体溶于水后过滤,不溶物必须经过洗涤,洗涤的具体操作是
将蒸馏水沿玻璃棒注入纸漏斗中,至刚好浸没沉淀,静置待水滤出,重复上述操作2~3次
将蒸馏水沿玻璃棒注入纸漏斗中,至刚好浸没沉淀,静置待水滤出,重复上述操作2~3次
.(4)通过实验数据分析29.2g残留固体中,含有哪几种固体?
C、Na2O和Na2CO3
C、Na2O和Na2CO3
.其中Na2CO3
Na2CO3
固体最大,为21.2
21.2
g(5)该探究条件下,钠与二氧化碳反应的化学方程式为
12Na+7CO2
3C+2Na2O+4Na2CO3
| ||
12Na+7CO2
3C+2Na2O+4Na2CO3
.
| ||