摘要:干电池 负极:________________, 正极:2NH4+ +2e-====2NH3+H2O H2+2MnO2====Mn2O3+H2O 4NH3+Zn2+==== [Zn(NH3)4]2+ 总反应式:________________,
网址:http://m.1010jiajiao.com/timu3_id_374138[举报]
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源.
请仔细观察下列两种电池的构造示意图,完成下列问题:
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大.试从影响反应速率的因素分析其原因是 .
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 .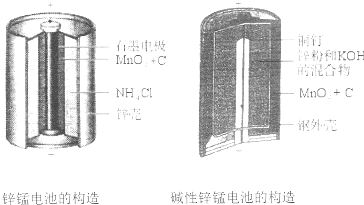
查看习题详情和答案>>
请仔细观察下列两种电池的构造示意图,完成下列问题:
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大.试从影响反应速率的因素分析其原因是
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为

某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
(5)根据以上的实验报告,关于滤液的成分,他的结论是:滤液中含有氯化铵和氯化锌若想从滤液中得到溶质固体,还应进行的操作是
查看习题详情和答案>>

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是
溶解
溶解
;操作②的名称是过滤
过滤
;(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、
坩埚
坩埚
、泥三角
泥三角
和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为碳
碳
.(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为
二氧化锰
二氧化锰
.(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中, 加入硝酸酸化的硝酸银溶液 加入硝酸酸化的硝酸银溶液 |
有白色沉淀产生 有白色沉淀产生 |
含有Cl- |
| 2.检验NH4+ | 取少许滤液于试管中, 加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 |
石蕊试纸变蓝色 石蕊试纸变蓝色 |
含有NH4+ |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
加热蒸发(加热浓缩),冷却结晶
加热蒸发(加热浓缩),冷却结晶
.若要将所得的溶质固体中的物质加以分离,可用加热
加热
法.
某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
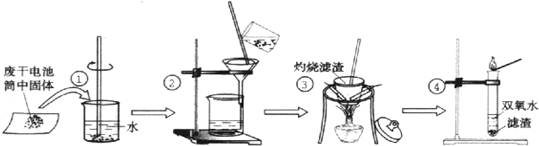
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是 ;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、 、泥三角和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种无色无味能使澄清石灰水变浑浊的气体,由此推测灼烧前的滤渣中存在的物质有 .
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为 .
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
查看习题详情和答案>>

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中, |
含有Cl- | |
| 2.检验NH4+ | 取少许滤液于试管中, |
含有NH4+ | |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
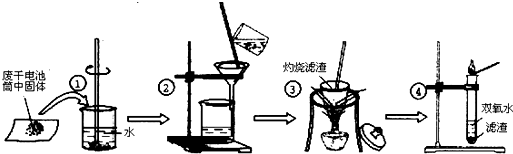
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是 ;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、 、泥三角和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种无色无味能使澄清石灰水变浑浊的气体,由此推测灼烧前的滤渣中存在的物质有 .
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为 ,操作④相关的化学方程式为 .
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4+,该同学取少许滤液于试管中, (填写操作与现象),则证实滤液中含有NH4+.
(5)该同学利用在废旧干电池中回收的Zn片和石墨电极,设计一个原电池实验,比较铜与锌的金属活动性强弱.
限用材料:铜片、锌片、石墨电极、稀硫酸、CuSO4溶液、ZnSO4溶液;
限用仪器:直流电源、导线、烧杯、试管、盐桥等中学化学常见的药品和仪器
请在下面的方框中画出实验装置图(要求标注各电极和电解质溶液名称),并写出正极方程式.

正极方程式: .
查看习题详情和答案>>

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4+,该同学取少许滤液于试管中,
(5)该同学利用在废旧干电池中回收的Zn片和石墨电极,设计一个原电池实验,比较铜与锌的金属活动性强弱.
限用材料:铜片、锌片、石墨电极、稀硫酸、CuSO4溶液、ZnSO4溶液;
限用仪器:直流电源、导线、烧杯、试管、盐桥等中学化学常见的药品和仪器
请在下面的方框中画出实验装置图(要求标注各电极和电解质溶液名称),并写出正极方程式.

正极方程式:
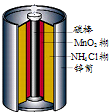 最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解.一般认为,放电时,电池中的反应如图:
最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解.一般认为,放电时,电池中的反应如图: