摘要:28.(1)H2SO4+Na2SO3=Na2SO4+SO2↑+H2O (2)B.D.F. (3)B管恢复为红色.C管红色变浅甚至褪为无色, SO2与品红生成的无色物质不稳定.受热易分解. (4)H2S, SO2+2OH-=SO32-+H2O SO2压出导管与烧杯中的NaOH溶液接触被迅速吸收.使烧瓶内产生负压.从而产生“喷泉 现象.
网址:http://m.1010jiajiao.com/timu3_id_370048[举报]
 由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:
由正丁醇(用n-C4H9OH表示)制备正溴丁烷(沸点:101.6℃)的反应如下:n-C4H9OH+NaBr+H2SO4→n-C4H9Br+NaHSO4+H2O
副反应:n-C4H9OH
| 浓H2SO4 |
| △ |
2n-C4H9OH
| ||
| △ |
3H2SO4(浓)+2NaBr(固)═2NaHSO4+Br2↑+SO2↑+2H2O
已知反应物及其用量:固体NaBr0.24mol,n-C4H9OH0.20mol,浓H2SO429mL,H2O20mL.
制备过程经历如下五个步骤,试回答下列问题:
1.投料:在圆底烧瓶中加入20mL水,再慢慢加入29mL浓硫酸,混合均匀并冷却至室温后,再依次加入0.20mol正丁醇(约18mL)和0.24mol溴化钠,充分振荡后加入几粒沸石.
(1)冷却至室温后再加正丁醇和溴化钠的目的是
A.减少HBr的挥发B.防止正丁醇的挥发
C.防止溴化钠被氧化D.防止温度过高导致炭化结焦
(2)本反应中硫酸与溴化作作用生成氢溴酸,氢溴酸与正丁醇作用发生取代反应生成正溴丁烷.硫酸的用量和浓度过大都对本制备不利的主要原因是
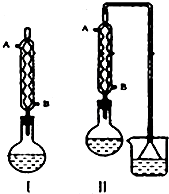
2.加热回流:反应装置选择Ⅱ而不选择Ⅰ的原因是
3.分离粗产物:反应结束待反应液冷却后,用直形冷凝管换下球形冷凝管,将其变为蒸馏装置进行蒸馏,得到的粗产物中除主产品外,还含下列选项中的
①C4H9OH ②SO2 ③(C4H9)2O ④Br2⑤NaHSO4 ⑥H2O ⑦H2SO4
4.洗涤粗产物:将馏出液移至分液漏斗中,加入等体积的水洗涤后,分液得有机层.如果不能判断哪层是有机层,可以用
5.收集产物:将干燥好的产物移至小蒸馏瓶中,加热蒸馏,收集99-103℃的馏分.要证明最终产物是n-C4H9Br,方法是
用H2C2O4?2H2O滴加浓H2SO4制备CO,通入灼热的铁氧化粉末中,做炼铁实验.但此法制备的CO中含有其他气体,必须除去.现有下列装置:

根据题目要求,回答下列问题:
(1)写出H2C2O4?2H2O在浓硫酸催化作用下制备CO的化学方程式.
(2)用a~h表示连接顺序,正确顺序为a
(3)用A~F正确表示下面实验操作的先后顺序:
A.点燃甲装置的酒精灯,打开分液漏斗,调节浓硫酸的滴速.
B.点燃乙装置中的酒精灯,加热氧化铁.
C.检查整套装置的气密性.
D.将导管口i处的尾气验纯后,点燃加以处理.
E.待乙装置玻璃管内的Fe2O3完全变黑时,熄灭乙装置中的酒精灯.
F.关好甲装置中分液漏斗的开关后,再熄灭该装置中的酒精灯.
(4)空洗气瓶的作用是
(5)假设H2C2O4?2H2O的分解产物以气体形式从a处导出,则该混合气体的平均摩尔质量为
(6)假设乙中所装为铁氧化物的混合物,可能是FeO、Fe2O3、Fe3O4的任意组合,现取a克混合物充分反应后,质量减轻了
克,通过计算确定该混合物中三种氧化物的物质的量的关系是:
查看习题详情和答案>>

根据题目要求,回答下列问题:
(1)写出H2C2O4?2H2O在浓硫酸催化作用下制备CO的化学方程式.
H2C2O4?2H2O
CO↑+CO2↑+3H2O
| ||
| △ |
H2C2O4?2H2O
CO↑+CO2↑+3H2O
;
| ||
| △ |
(2)用a~h表示连接顺序,正确顺序为a
deg fcbh
deg fcbh
i.(3)用A~F正确表示下面实验操作的先后顺序:
CADBEF
CADBEF
.A.点燃甲装置的酒精灯,打开分液漏斗,调节浓硫酸的滴速.
B.点燃乙装置中的酒精灯,加热氧化铁.
C.检查整套装置的气密性.
D.将导管口i处的尾气验纯后,点燃加以处理.
E.待乙装置玻璃管内的Fe2O3完全变黑时,熄灭乙装置中的酒精灯.
F.关好甲装置中分液漏斗的开关后,再熄灭该装置中的酒精灯.
(4)空洗气瓶的作用是
防倒吸
防倒吸
,浓硫酸洗气瓶的作用是干燥CO
干燥CO
.(5)假设H2C2O4?2H2O的分解产物以气体形式从a处导出,则该混合气体的平均摩尔质量为
25.2g/mol
25.2g/mol
.(6)假设乙中所装为铁氧化物的混合物,可能是FeO、Fe2O3、Fe3O4的任意组合,现取a克混合物充分反应后,质量减轻了
| 8a |
| 29 |
n(FeO):n(Fe2O3)=1:1,n(Fe3O4)≥0;72n(FeO)+160n(Fe2O3)+232n(Fe3O4)=a
n(FeO):n(Fe2O3)=1:1,n(Fe3O4)≥0;72n(FeO)+160n(Fe2O3)+232n(Fe3O4)=a
. ⅠA、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:
ⅠA、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:(1)各元素的符号:
A:
Si
Si
,B:N
N
,C:S
S
,D:As
As
,X:P
P
.(2)写出C、D、X最高价氧化物对应水化物的化学式,并排列酸性由强到弱的顺序:
H2SO4>H3PO4>H3AsO4
H2SO4>H3PO4>H3AsO4
.(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:
NH3>PH3>SiH4
NH3>PH3>SiH4
.ⅡFe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液),
(1)该反应的平衡常数K的表达式为:K=
| c2(Fe2+)×c(I2) |
| c2(I-)×c2(Fe3+) |
| c2(Fe2+)×c(I2) |
| c2(I-)×c2(Fe3+) |
[物质的浓度用“c(物质)”表示].当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡
向右
向右
移动(填“向右”、“向左”、“不”).(2)上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
| c(I-)(mol/L) | c(Fe3+)(mol/L) | v[mol/(L?s)] | |
| (1) | 0.20 | 0.80 | 0.032K |
| (2) | 0.60 | 0.40 | 0.144K |
| (3) | 0.80 | 0.20 | 0.128K |
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为
C
C
.A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
②I-浓度对反应速率的影响
>
>
Fe3+浓度对反应速率的影响(填“>”、“<”或“=”).(2013?江苏二模)过氧化钙晶体[CaO2?8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液.广泛应用于环境杀菌、消毒等领域.
★过氧化钙晶体的制备
工业上生产CaO2?8H2O的主要流程如下:

(1)用上述方法制取CaO2?8H2O的化学方程式是
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
①
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol?L-1 H2SO4,用0.0200mol?L-1KMnO4标准溶液滴定至终点.重复上述操作两次.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为
(4)根据表1数据,计算产品中CaO2?8H2O的质量分数(写出计算过程)
表1.KMnO4标准溶液滴定数据
查看习题详情和答案>>
★过氧化钙晶体的制备
工业上生产CaO2?8H2O的主要流程如下:

(1)用上述方法制取CaO2?8H2O的化学方程式是
CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O↓+2NH4Cl
CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O↓+2NH4Cl
.(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
①
温度低可减少过氧化氢的分解,提高过氧化氢的利用率(或防止过氧化氢的分解)
温度低可减少过氧化氢的分解,提高过氧化氢的利用率(或防止过氧化氢的分解)
;②通入过量NH3使溶液呈碱性,抑制CaO2?8H2O的溶解(或使溶液呈碱性,减少CaO2?8H2O的溶解,或提高产品的产率.意思相近均给分)
通入过量NH3使溶液呈碱性,抑制CaO2?8H2O的溶解(或使溶液呈碱性,减少CaO2?8H2O的溶解,或提高产品的产率.意思相近均给分)
.★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol?L-1 H2SO4,用0.0200mol?L-1KMnO4标准溶液滴定至终点.重复上述操作两次.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为
当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色
当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色
.(4)根据表1数据,计算产品中CaO2?8H2O的质量分数(写出计算过程)
表1.KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
根据关系式:5(CaO2?8H2O)~5H2O2~2KMnO4;n(KMnO4)=
n(CaO2?8H2O)=
×0.0200 mol?L-1×23.03mL×10-3L?mL-1=1.151×10-3 mol、故 CaO2?8H2O的质量分数为:
×100%=82.91%.
| 5 |
| 2 |
| 5 |
| 2 |
| 1.51×10-3mol×216g?mol-1 |
| 0.3000g |
根据关系式:5(CaO2?8H2O)~5H2O2~2KMnO4;n(KMnO4)=
n(CaO2?8H2O)=
×0.0200 mol?L-1×23.03mL×10-3L?mL-1=1.151×10-3 mol、故 CaO2?8H2O的质量分数为:
×100%=82.91%.
.| 5 |
| 2 |
| 5 |
| 2 |
| 1.51×10-3mol×216g?mol-1 |
| 0.3000g |
 硼是一种重要的非金属元素,单质硼可以通过硼镁矿Mg2B2O5?H2O来制取.
硼是一种重要的非金属元素,单质硼可以通过硼镁矿Mg2B2O5?H2O来制取.第①步:将硼镁矿用浓碱NaOH溶液溶解,过滤得NaBO2溶液.
第②步:将NaBO2浓缩后通入CO2调节碱度,结晶析出硼砂Na2B4O7?10H2O.
第③步:将硼砂溶于水后,用H2SO4调节酸度,过滤得H3BO3晶体.
第④步:加热硼酸使之脱水生成氧化物.
第⑤步:脱水产物用镁还原即得粗单质硼.请回答下列问题:
(1)第①步和第⑤步的化学方程式分别为
(2)将制得的粗硼在一定条件下反应全部生成BI3,然后BI3热分解可以得到纯净的单质硼.0.20g粗硼制成的BI3分解得到的I2全部被收集后,用 2.00mol/LNa2S2O3溶液滴定,用去27.00mL Na2S2O3溶液(已知:I2+2S2O32-=2I-+S4O62-).
①Na2S2O3溶液成碱性,用离子方程式表达其原因
②粗硼中硼的含量为
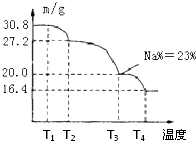
(3)上述制得的硼砂晶体(Na2B4O7?10H2O)还可制备过硼酸钠,它是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中.已知纯品过硼酸钠晶体中各元素的物质的量之比为n(Na):n(B):n(H):n(O)=1:1:n:7.将制得的纯品样品在70℃以上加热将逐步失去结晶水,测得纯品质量随温度的变化如下图所示,则T3时所得晶体的化学式为: