摘要:24.. 如图所示.倾角=30°.宽度L=1m的足够长为U形平行光滑金属导轨固定在磁感应强度B=1T.范围充分大的匀强磁场中.磁场方向垂直导轨平面斜向上.现用一平行导轨的牵引力F.牵引一根质量m=0.2kg.电阻R=1.垂直导轨的金属棒ab.由静止沿导轨向上移动(ab棒始终与导轨接触良好且垂直.不计导轨电阻及一切摩擦).问: (1)若牵引力为恒力.且F=9N.求金属棒达到的稳定速度v1 (2)若牵引力功率恒为72W.求金属棒达到的稳定速度v2 (3)若金属棒受向上拉力在斜面导轨上达到某一速度时. 突然撒力.此后金属棒又前进了0.48m ,其间.即从撒力 至棒速为0时止.金属棒发热1.12J.问撒力时棒速v3多大?
网址:http://m.1010jiajiao.com/timu3_id_370035[举报]
某学生设计了以下实验方案,探究铜和一定量(10mL)浓HNO3反应中是否产生NO气体,实验装置如图所示(装置的气密性良好),请回答下列问题:
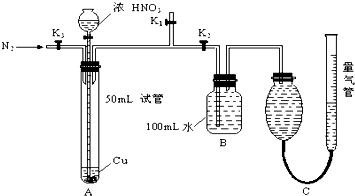
(1)在反应前通入N2的作用是 ,进行这步操作时应关闭 而打开 (填K1、K2、K3).
(2)反应结束后,通过分液漏斗向试管中加40mL蒸馏水,再从B装置所得100mL溶液中取出25.00mL,加2滴酚酞试液,用0.1000mol/L的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则B容器中所得HNO3的物质的量是 ,B中生成硝酸的同时会生成NO mL(标准状况).
(3)用C装置读取排出水的体积时,应注意 、 .
(4)若不考虑实验前后导管中的气体,C装置的气体中至少含N2 mL.若由C装置测得所收集到的气体体积为143.0mL(已折算成标准状况),请你判断铜和一定量浓HNO3反应过程中是否有NO生成?如果有,写出判断的依据;如果没有,写出理由. .
查看习题详情和答案>>

(1)在反应前通入N2的作用是
(2)反应结束后,通过分液漏斗向试管中加40mL蒸馏水,再从B装置所得100mL溶液中取出25.00mL,加2滴酚酞试液,用0.1000mol/L的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则B容器中所得HNO3的物质的量是
(3)用C装置读取排出水的体积时,应注意
(4)若不考虑实验前后导管中的气体,C装置的气体中至少含N2
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验中可以用如图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).请填写下列空白:
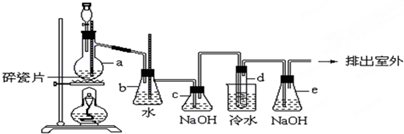
(1)写出制备1,2-二溴乙烷的化学方程式: .
(2)请写出烧瓶a中发生反应的化学方程式:
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象: .
(4)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因. .
(5)c装置内NaOH溶液的作用是 ;e装置内NaOH溶液的作用是 .
查看习题详情和答案>>

(1)写出制备1,2-二溴乙烷的化学方程式:
(2)请写出烧瓶a中发生反应的化学方程式:
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象:
(4)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因.
(5)c装置内NaOH溶液的作用是
A是一种信息材料的添加剂,在相同条件下,A蒸气的质量是同体积氢气质量的88.25倍.在A分子中各元素质量分数分别为w(C)=54.4%,w(H)=7.4%,w(O)=18.1%,w(Cl)=20.1%,A在不同条件下可发生如图所示的一系列变化.

请回答下列问题:
(1)A的分子式为
(2)D分子含有的官能团是
(3)上述转换关系的化学方程式中,属于水解反应的有
(4)写出化学方程式:
①A和稀硫酸共热:
②E氧化成G:
③F与氢氧化钠醇溶液共热:
(5)与B互为同分异构体的且属于链状酯的物质共有
查看习题详情和答案>>

请回答下列问题:
(1)A的分子式为
C8H13O2Cl
C8H13O2Cl
.(2)D分子含有的官能团是
羟基、氯原子
羟基、氯原子
.(3)上述转换关系的化学方程式中,属于水解反应的有
3
3
个(填数字).(4)写出化学方程式:
①A和稀硫酸共热:
CH2=C(CH3)COOCH2CH(CH3)CH2Cl+H2O
CH2=C(CH3)COOH+ClCH2CH(CH3)CH2OH
| 稀硫酸 |
| △ |
CH2=C(CH3)COOCH2CH(CH3)CH2Cl+H2O
CH2=C(CH3)COOH+ClCH2CH(CH3)CH2OH
;| 稀硫酸 |
| △ |
②E氧化成G:
CH3CH(CH2OH)2+2CuO
CH3CH(CHO)2+2Cu+2H2O
| △ |
CH3CH(CH2OH)2+2CuO
CH3CH(CHO)2+2Cu+2H2O
;| △ |
③F与氢氧化钠醇溶液共热:
CH3CH(CH2Cl)COOOH+2NaOH
CH2=C(CH3)COOONa+NaCl+2H2O
| 醇 |
| △ |
CH3CH(CH2Cl)COOOH+2NaOH
CH2=C(CH3)COOONa+NaCl+2H2O
.| 醇 |
| △ |
(5)与B互为同分异构体的且属于链状酯的物质共有
5
5
种. 已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:
2F2+2H2O=4HF+O2
2F2+2H2O=4HF+O2
;(2)若B是一种四核含18电子的分子,D是一种气态单质分子,则A的化学式为
N2H4
N2H4
,B的结构式为H-O-O-H
H-O-O-H
;(3)若A、B均是含2个原子的微粒,其中B中含有10个电子,D中含有l8个电子,则A、B之间发生反应的离子方程式为
HS-+OH-=S2-+H2O
HS-+OH-=S2-+H2O
;(4)若D是一种含有22个电子的分子,则符合如图所示关系的A的物质有
CH3OH、CH3-CH3
CH3OH、CH3-CH3
(写化学式,如果是有机物则写相应的结构简式).