摘要:23] 3NO2+H2O=2HNO2+NO 2NO+O2=2NO2 Fe3++3OH-=Fe(OH)3↓ (3)白色沉淀先变成灰绿色.最后变成红褐色 (4)1.25moL/L
网址:http://m.1010jiajiao.com/timu3_id_36911[举报]
利用化工厂生产硼砂的废渣--硼镁泥可制取七水硫酸镁(MgSO4?7H2O),硼镁泥的主要成分是MgCO3,还含有其它杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等).
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |

根据以上流程图并参考pH数据和溶解度数据,试回答下列问题:
(1)硼镁泥加入浓硫酸时,FeO发生的变化是______(选填序号).
a.被钝化 b.被氧化 c.被溶解
(2)往过滤Ⅰ得到的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液可将溶液中的Mn2+氧化成MnO2,该反应的离子反应方程式为______.加热煮沸的目的是_______.
(3)沉淀B中除MnO2外还含有______(填化学式)等物质.
(4)沉淀C的化学式是______;产生沉淀C的操作需趁热进行的原因是______;洗涤沉淀需要的玻璃仪器有:烧杯、______;若用乙醇代替水作洗涤剂洗涤沉淀C,原因是______.
(5)过滤出MgSO4?7H2O晶体的滤液中含有的金属阳离子有______,生产中对该滤液的处理方法是______;检验滤液是否含有SO42-操作是______. 查看习题详情和答案>>
利用化工厂生产硼砂的废渣--硼镁泥可制取七水硫酸镁,硼镁泥的主要成分是MgCO3,还含有其它杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等).
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
表2 两种盐的溶解度(g/100g水)
硼镁泥制取七水硫酸镁的工艺流程如下:
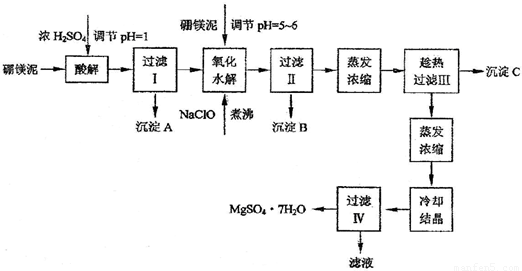
根据以上流程图并参考pH数据和溶解度数据,试回答下列问题:
(1)硼镁泥加入浓硫酸时,FeO发生的变化是______(选填序号).
a.被钝化 b.被氧化 c.被溶解
(2)往过滤Ⅰ得到的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液可将溶液中的Mn2+氧化成MnO2,该反应的离子反应方程式为______.加热煮沸的目的是_______.
(3)沉淀B中除MnO2外还含有______(填化学式)等物质.
(4)沉淀C的化学式是______;产生沉淀C的操作需趁热进行的原因是______;洗涤沉淀需要的玻璃仪器有:烧杯、______;若用乙醇代替水作洗涤剂洗涤沉淀C,原因是______.
(5)过滤出MgSO4?7H2O晶体的滤液中含有的金属阳离子有______,生产中对该滤液的处理方法是______;检验滤液是否含有SO42-操作是______.
查看习题详情和答案>>
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |

根据以上流程图并参考pH数据和溶解度数据,试回答下列问题:
(1)硼镁泥加入浓硫酸时,FeO发生的变化是______(选填序号).
a.被钝化 b.被氧化 c.被溶解
(2)往过滤Ⅰ得到的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液可将溶液中的Mn2+氧化成MnO2,该反应的离子反应方程式为______.加热煮沸的目的是_______.
(3)沉淀B中除MnO2外还含有______(填化学式)等物质.
(4)沉淀C的化学式是______;产生沉淀C的操作需趁热进行的原因是______;洗涤沉淀需要的玻璃仪器有:烧杯、______;若用乙醇代替水作洗涤剂洗涤沉淀C,原因是______.
(5)过滤出MgSO4?7H2O晶体的滤液中含有的金属阳离子有______,生产中对该滤液的处理方法是______;检验滤液是否含有SO42-操作是______.
查看习题详情和答案>>
中学常见反应的化学方程式是A+B----->X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则Y的化学式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
查看习题详情和答案>>
(1)若Y是黄绿色气体,则Y的化学式是
Cl2
Cl2
.(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
C+2H2SO4
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4
CO2↑+2SO2↑+2H2O
,则反应中氧化剂与还原剂的物质的量之比是
| ||
2:1
2:1
.(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
Al
Al
(填化学式),其所在周期表中的位置为:第三周期,ⅢA族
第三周期,ⅢA族
(填所在周期和族);A与NaOH反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(2013?辽宁一模)已知物质A、B、C、D、E是由短周期元素构戚的单质或化合物,它们可发生如图所示的转化关系
(1)若条件①为点燃,目前60%的B都是从海水中提取的,气体D可以使湿润的红色石蕊试纸变蓝,写出C与H2O反应的化学方程式
上世纪60年代就有人将气体D作为燃料电池的燃料源进行了试验,制成D-空气燃料电池系统,总反应式为:D+O2→A+H2O(未配平),写出此碱性燃料电池的负极反应式:
(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,写出D与NaOH等物质的量混合的离子方程式:
(3)若条件①为常温,B和D为同-种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的浓溶液在加热条件下反应的化学方程式:
已知常温下A与B反应生成1molC的焓变为-57.07kJ/mol,1molC与H2O反应生成气体D和E溶液的焓变为-46kJ/mol,写出A、B与水反应生成E溶液的热化学方程式:
查看习题详情和答案>>

(1)若条件①为点燃,目前60%的B都是从海水中提取的,气体D可以使湿润的红色石蕊试纸变蓝,写出C与H2O反应的化学方程式
Mg3N2+6H2O=3Mg(OH)2+2NH3↑
Mg3N2+6H2O=3Mg(OH)2+2NH3↑
.上世纪60年代就有人将气体D作为燃料电池的燃料源进行了试验,制成D-空气燃料电池系统,总反应式为:D+O2→A+H2O(未配平),写出此碱性燃料电池的负极反应式:
2NH3+6OH--6e-=N2↑+6H2O
2NH3+6OH--6e-=N2↑+6H2O
.(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,写出D与NaOH等物质的量混合的离子方程式:
H2S+OH-=HS-+H2O
H2S+OH-=HS-+H2O
.(3)若条件①为常温,B和D为同-种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的浓溶液在加热条件下反应的化学方程式:
Fe+6HNO3(浓)
Fe(NO3)3+3NO2↑+3H2O
| ||
Fe+6HNO3(浓)
Fe(NO3)3+3NO2↑+3H2O
;
| ||
已知常温下A与B反应生成1molC的焓变为-57.07kJ/mol,1molC与H2O反应生成气体D和E溶液的焓变为-46kJ/mol,写出A、B与水反应生成E溶液的热化学方程式:
4NO(g)+3O2(g)+2H2O(l)=4HNO3(aq)△H=-618.42kJ/mol
4NO(g)+3O2(g)+2H2O(l)=4HNO3(aq)△H=-618.42kJ/mol
.