题目内容
中学常见反应的化学方程式是A+B----->X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则Y的化学式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
(1)若Y是黄绿色气体,则Y的化学式是
Cl2
Cl2
.(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
C+2H2SO4
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4
CO2↑+2SO2↑+2H2O
,则反应中氧化剂与还原剂的物质的量之比是
| ||
2:1
2:1
.(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
Al
Al
(填化学式),其所在周期表中的位置为:第三周期,ⅢA族
第三周期,ⅢA族
(填所在周期和族);A与NaOH反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.分析:(1)若Y是黄绿色气体为Cl2,A、B的物质的量之比为1:4,判断反应是实验室制氯气;
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,判断为C,B的溶液为浓硫酸,化学方程式为:C+2H2SO4
CO2↑+2SO2↑+2H2O;反应中氧化剂(H2SO4)与还原剂(C)的物质的量之比为:2:1;
(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中,判断A为Al,在周期表中的位置:第三周期,ⅢA族;A与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,判断为C,B的溶液为浓硫酸,化学方程式为:C+2H2SO4
| ||
(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中,判断A为Al,在周期表中的位置:第三周期,ⅢA族;A与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
解答:解:(1)A+B----->X+Y+H2O,A、B的物质的量之比为1:4,若Y是黄绿色气体为Cl2,故答案为:Cl2
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,判断为碳,碳和浓硫酸反应的化学方程式为:C+2H2SO4
CO2↑+2SO2↑+2H2O;反应中氧化剂与还原剂的物质的量之比为2:1;
故答案为:C+2H2SO4
CO2↑+2SO2↑+2H2O;2:1;
(3)若A为金属单质,为短周期元素,且A可溶于NaOH溶液中,说明A为Al,Al在周期表中的位置为:第三周期 IIIA族、铝和氢氧化钠溶液反应的化学方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
故答案为:第三周期 IIIA族;2Al+2OH-+2H2O═2AlO2-+3H2↑;
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,判断为碳,碳和浓硫酸反应的化学方程式为:C+2H2SO4
| ||
故答案为:C+2H2SO4
| ||
(3)若A为金属单质,为短周期元素,且A可溶于NaOH溶液中,说明A为Al,Al在周期表中的位置为:第三周期 IIIA族、铝和氢氧化钠溶液反应的化学方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
故答案为:第三周期 IIIA族;2Al+2OH-+2H2O═2AlO2-+3H2↑;
点评:本题考查了物质转化关系的推断和物质性质的综合应用,原子结构的判断,碳、铝等物质的化学性质特征的应用,较简单.

练习册系列答案
相关题目
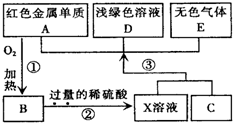
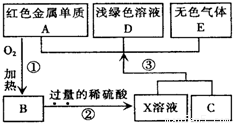
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答: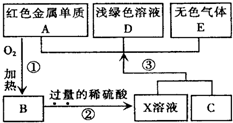 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答: