摘要: 在0.1mol/LCH3COOH溶液中存在如下电离平衡: CH3COOH====CH3COO-+H+ 对于该平衡.下列叙述正确的是 A 加入水时.平衡向逆反应方向移动 B 加入少量NaOH固体.平衡向正反应方向移动C 加入少量0.1mol/LHCl溶液.溶液中c(H+)减小 D 加入少量CH3COONa固体.平平衡向正反应方向移动
网址:http://m.1010jiajiao.com/timu3_id_36501[举报]
下列说法正确的是( )
| A、在0.1mol?L-1 Na2CO3溶液中,加两滴酚酞显浅红色,微热后红色加深,说明盐类水解反应是吸热反应 | ||||||||||
| B、已知MgCO3的Ksp=6.82×l0-6,则在含有固体MgCO3的MgCl2、Na2CO3溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2?L-2 | ||||||||||
| C、等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB | ||||||||||
D、已知:
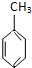 (g)+3H2(g)→ (g)+3H2(g)→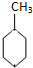 (g)的△H (g)的△H |
 H++A2-(Ka2=1.0×10-2),下列说法正确的是( )
H++A2-(Ka2=1.0×10-2),下列说法正确的是( )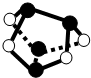 NA表示阿伏加德罗常数的值,下列说法正确的是( )
NA表示阿伏加德罗常数的值,下列说法正确的是( )