摘要:2.化学实验必须注意安全.下列做法存在安全隐患的是A ①蒸馏石油时.加热一段时间后发现未加碎瓷片.立刻拔开橡皮塞并投入碎瓷片 ②实验室做钠的实验时.余下的钠屑投入到废液缸中 ③配制浓硫酸与酒精混合液时.将1体积的酒精倒入3体积的浓硫酸中 ④皮肤上沾有少量浓硝酸时.立刻用大量水冲洗.再涂上稀碳酸氢钠溶液 ⑤制乙烯时.用量程为300℃的温度计代替量程为200℃的温度计.测反应液的温度 A.①②③ B.④⑤ C.②③④⑤ D.①②④
网址:http://m.1010jiajiao.com/timu3_id_364796[举报]
(2006?揭阳二模)粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;②
另取20g A全部溶于0.15L 6.0mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色.
请回答:
(1)①产物中的单质B是
(2)②中所发生的各反应的化学方程式是
(3)③中所发生的各反应的离子方程式是
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为
查看习题详情和答案>>
①取适量A进行铝热反应,产物中有单质B生成;②
另取20g A全部溶于0.15L 6.0mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色.
请回答:
(1)①产物中的单质B是
Fe
Fe
.(2)②中所发生的各反应的化学方程式是
MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O
MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O
.(3)③中所发生的各反应的离子方程式是
Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+
Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+
.(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为
0.67mol/L
0.67mol/L
,c(Fe2+)为2.33mol/L
2.33mol/L
.(2006?揭阳二模)在某密闭容器中投入X、Y进行如下反应:X(g)+2Y(g) 2Z(g),若要使平衡时反应物总物质的量与生成物总物质的量相等,则X、Y的初始物质的量x、y之比应满足( )
2Z(g),若要使平衡时反应物总物质的量与生成物总物质的量相等,则X、Y的初始物质的量x、y之比应满足( )
 2Z(g),若要使平衡时反应物总物质的量与生成物总物质的量相等,则X、Y的初始物质的量x、y之比应满足( )
2Z(g),若要使平衡时反应物总物质的量与生成物总物质的量相等,则X、Y的初始物质的量x、y之比应满足( )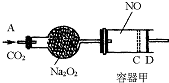 (2006?揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的
(2006?揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的| 9 | 10 |
已知:2Na2O2+2CO2→2Na2CO3+O2
(1)已知当活塞移至C处时,干燥管中物质的质量增加了2.24g.
①此时,通入标准状况下的CO2气体多少L?
②容器甲中NO2转化为N2O4的转化率是多少?
③活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处.则a值必
小于
小于
0.01(填大于、小于、等于),其理由是活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2?N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.01 mol,因此所需CO2必小于0.01 mol
活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2?N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.01 mol,因此所需CO2必小于0.01 mol
.(2)若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入的量CO2,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量最小值应大于
1.56
1.56
g. (2013?盐城二模)以0.1000mol?L-1 NaOH溶液滴定c mol?L-1,某弱酸HA溶液,其滴定曲线如图所示,下列说法正确的是( )
(2013?盐城二模)以0.1000mol?L-1 NaOH溶液滴定c mol?L-1,某弱酸HA溶液,其滴定曲线如图所示,下列说法正确的是( )