摘要:同周期.同主族元素性质的递变规律 同周期(左右) 同主族(上下) 原子结构 核电荷数 逐渐增大 增大 电子层数 相同 增多 原子半径 逐渐减小 逐渐增大 化合价 最高正价由+1+7负价数=8-族序数 最高正价和负价数均相同.最高正价数=族序数 元素的金属性和非金属性 金属性逐渐减弱.非金属性逐渐增强. 金属性逐渐增强.非金属性逐渐减弱. 单质的氧化性和还原性 氧化性逐渐增强.还原性逐渐减弱. 氧化性逐渐减弱.还原性逐渐增强. 最高价氧化物的水化物的酸碱性 酸性逐渐增强.碱性逐渐减弱. 酸性逐渐减弱.碱性逐渐增强. 气态氢化物的稳定性.还原性.水溶液的酸性. 稳定性逐渐增强.还原性逐渐减弱.酸性逐渐增强. 稳定性逐渐减弱.还原性逐渐增强.酸性逐渐减弱.
网址:http://m.1010jiajiao.com/timu3_id_363467[举报]
元素周期表揭示了许多元素的相似性和递变规律,同一周期元素构成的某些微粒往往具有相同的电子数,周期表中主族元素可以构成许多电子数为10或18的微粒.如下列周期表中所示的一些分子或离子.
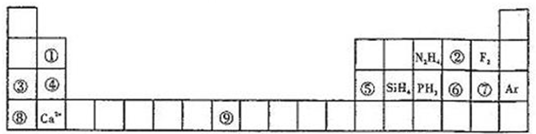
(1)写出⑨元素的原子核外电子排布式______.
(2)比较③、⑤分别与⑦形成的化合物水溶液的pH大小______>______(写化学式).
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式______.
(4)含有⑥元素的某种18电子的离子和H+及OH-均可发生反应,分别写出反应的离子方程式:
______,______.
查看习题详情和答案>>

(1)写出⑨元素的原子核外电子排布式______.
(2)比较③、⑤分别与⑦形成的化合物水溶液的pH大小______>______(写化学式).
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式______.
(4)含有⑥元素的某种18电子的离子和H+及OH-均可发生反应,分别写出反应的离子方程式:
______,______.
元素周期表中同周期、同主族元素的原子结构及性质的递变规律:
项目 | 同周期(左→右) | 同主族(上→下) | |
原子结构 | 核电荷数 | 逐渐__________ | 逐渐__________ |
电子层数 | __________ | 逐渐__________ | |
原子半径 | 逐渐__________ | 逐渐__________ | |
性质 | 化合价 | 最高正价由__________,负价数=__________ | 最高正价、负价数相同最高正价=__________ |
元素原子的得电子能力和失电子能力 | 失电子能力逐渐__________ 得电子能力逐渐__________ | 失电子能力逐渐__________ 得电子能力逐渐__________ | |
单质的氧化性、还原性 | 还原性__________ 氧化性__________ | 氧化性__________ 还原性__________ | |
最高价氧化物对应的水化物的酸碱性 | 碱性__________ 酸性__________ | 酸性__________ 碱性__________ | |
气态氢化物稳定性 | __________ | __________ | |
元素周期表揭示了许多元素的相似性和递变规律,同一周期元素构成的某些微粒往往具有相同的电子数,周期表中主族元素可以构成许多电子数为10或18的微粒.如下列周期表中所示的一些分子或离子.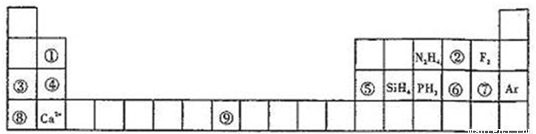
(1)写出⑨元素的原子核外电子排布式______.
(2)比较③、⑤分别与⑦形成的化合物水溶液的pH大小______>______(写化学式).
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式______.
(4)含有⑥元素的某种18电子的离子和H+及OH-均可发生反应,分别写出反应的离子方程式:
______,______.
查看习题详情和答案>>

(1)写出⑨元素的原子核外电子排布式______.
(2)比较③、⑤分别与⑦形成的化合物水溶液的pH大小______>______(写化学式).
(3)①元素与⑤元素的氢氧化物有相似的性质,写出①元素的氢氧化物与足量的NaOH溶液反应的化学方程式______.
(4)含有⑥元素的某种18电子的离子和H+及OH-均可发生反应,分别写出反应的离子方程式:
______,______.
查看习题详情和答案>>
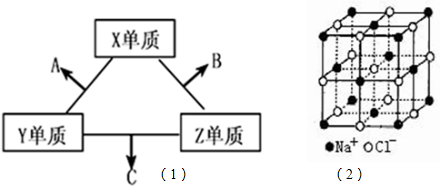
短周期元素在元素中占有重要地位.X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如(1)变化:
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.
查看习题详情和答案>>
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.

短周期元素在元素中占有重要地位.X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如(1)变化:
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.

查看习题详情和答案>>
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.

查看习题详情和答案>>