摘要:11.甲.乙.丙3 种元素.甲元素的+2价阳离子具有氩原子的电子层结构,乙元素比甲元素的原子少一个电子层.其离子带一个单位正电荷.它们均可跟17号元素丙化合.则甲丙组成的化合物为 ,乙丙组成的化合物为 ,两种化合物做焰色反应时.其焰色分别为 色和 色.
网址:http://m.1010jiajiao.com/timu3_id_362642[举报]
有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的
,乙元素原子核内无中子,丙元素原子核内有8个质子.
(1)写出丙元素的元素符号 .
(2)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式 .
(3)画出甲元素的原子结构示意图 .
查看习题详情和答案>>
| 1 | 2 |
(1)写出丙元素的元素符号
(2)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
(3)画出甲元素的原子结构示意图
甲、乙、丙、丁、戊都是单质,其中甲、乙、丙是常见金属,丁和戊是气体,且丁呈黄绿色.A~K是化合物.F是红褐色沉淀,G是淡黄色固体粉末,K是丁的气态氢化物.已知乙和丙在周期表中位于同一周期,且丙原子最外能层电子构型为ns1.它们之间有如图1的转化关系(部分反应物或产物省略).
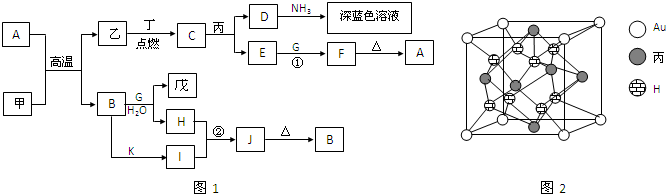
回答以下问题:
(1)G的电子式:
 ,深蓝色溶液中溶质的化学式:
,深蓝色溶液中溶质的化学式:
(2)甲与同周期的金属元素相比,第一电离能由小到大的顺序是
(3)完成反应方程式
反应①中,E和G的物质的量之比为2:1:
反应②的离子方程式:
(4)乙的高价阳离子的最高能级电子排布图为:
 .检验该离子常用KSCN溶液.乙的高价阳离子与SCN-可形成配位数不同的多种配合物.在含0.01molC的溶液中,加入100mL0.34mol?L-1的KSCN溶液,所得配合物是下列中的
.检验该离子常用KSCN溶液.乙的高价阳离子与SCN-可形成配位数不同的多种配合物.在含0.01molC的溶液中,加入100mL0.34mol?L-1的KSCN溶液,所得配合物是下列中的
①[Fe(SCN)]2+;②[Fe(SCN)2]+;③Fe(SCN)3;④[Fe(SCN)4]-;⑤[Fe(SCN)5]2-;⑥[Fe(SCN)6]3-
(5)丙的基态原子电子排布式为
查看习题详情和答案>>

回答以下问题:
(1)G的电子式:


[Cu(NH3)4]Cl2
[Cu(NH3)4]Cl2
.(2)甲与同周期的金属元素相比,第一电离能由小到大的顺序是
Na<Al<Mg
Na<Al<Mg
(用元素符号表示).(3)完成反应方程式
反应①中,E和G的物质的量之比为2:1:
3Na2O2+6FeCl2+6H2O=4Fe(OH)3+2FeCl3+6NaCl
3Na2O2+6FeCl2+6H2O=4Fe(OH)3+2FeCl3+6NaCl
;反应②的离子方程式:
3AlO2-+Al3++6H2O=4Al(OH)3↓
3AlO2-+Al3++6H2O=4Al(OH)3↓
.(4)乙的高价阳离子的最高能级电子排布图为:


③④
③④
(选填序号),其物质的量之比为3:2
3:2
.①[Fe(SCN)]2+;②[Fe(SCN)2]+;③Fe(SCN)3;④[Fe(SCN)4]-;⑤[Fe(SCN)5]2-;⑥[Fe(SCN)6]3-
(5)丙的基态原子电子排布式为
1s22s22p63s23p63d104s1或[Ar]3d104s1
1s22s22p63s23p63d104s1或[Ar]3d104s1
.丙与金形成的一种合金晶体具有立方最密堆积的结构,这种晶体具有储氢功能,氢原子可进入到由丙原子与Au原子构成的四面体空隙中.其晶胞结构如图2所示.这种合金晶体储氢后的化学式应为AuCu3H8
AuCu3H8
.甲、乙、丙、丁、戊为五种短周期元素,且原子序数依次增大.甲与丁、丙与戊分别同主族,戊的原子最外层电子数比次外层少2个.甲与乙可以按照原子个数比3:1形成化合物A,且每个A分子中含有10个电子.请回答:
(1)戊的原子结构示意图是
 ,乙单质分子的电子式是
,乙单质分子的电子式是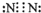
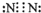 .
.
(2)A溶于水所得溶液呈碱性的原因是(用电离方程式表示)
(3)甲与丁可形成一种离子化合物,该化合物与H2O反应得到强碱溶液和H2,则该反应中,氧化剂与还原剂的物质的量之比是
(4)X、Y、Z为三种强电解质,分别由上述五种元素中的三种组成.X、Y、Z的稀溶液之间存在如下转化关系:
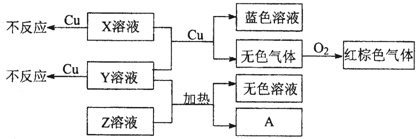
①Y、Z混合后加热得到A离子方程式是
②金属Cu与X、Y的混合溶液反应的离子方程式是
查看习题详情和答案>>
(1)戊的原子结构示意图是


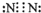
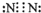
(2)A溶于水所得溶液呈碱性的原因是(用电离方程式表示)
NH3?H2O?NH4++OH-
NH3?H2O?NH4++OH-
.(3)甲与丁可形成一种离子化合物,该化合物与H2O反应得到强碱溶液和H2,则该反应中,氧化剂与还原剂的物质的量之比是
1:1
1:1
.(4)X、Y、Z为三种强电解质,分别由上述五种元素中的三种组成.X、Y、Z的稀溶液之间存在如下转化关系:

①Y、Z混合后加热得到A离子方程式是
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
;
| ||
②金属Cu与X、Y的混合溶液反应的离子方程式是
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大.甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍.在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
试回答:
(1)甲元素的名称为
 .
.
(2)A的电子式为
 ;所含化学键类型为
;所含化学键类型为
(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示)
(4)反应(I)的化学方程式为
(5)反应(II)的离子方程式为
查看习题详情和答案>>

试回答:
(1)甲元素的名称为
氢
氢
,溴元素在周期表的位置第四周期ⅦA族
第四周期ⅦA族
丁元素的阴离子结构示意图为

(2)A的电子式为


离子键和共价键
离子键和共价键
.(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示)
S2->O2->Na+
S2->O2->Na+
.(4)反应(I)的化学方程式为
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(5)反应(II)的离子方程式为
SO2+Br2+2H2O=4H++SO42--+2Br-
SO2+Br2+2H2O=4H++SO42--+2Br-
.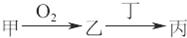 甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如图所示:
甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如图所示:(1)若乙是目前世界倡导需减少排放的温室气体,丁也含有A元素.则含有7个中子的核素A可用符号表示为
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件与氧气反应生成乙.若丁是稀盐酸,则乙→丙的化学方程式为