网址:http://m.1010jiajiao.com/timu3_id_362143[举报]
| A | |||||||||||||||||
| B | C | D | |||||||||||||||
| E | X | Y | |||||||||||||||
| Z | W |
(2)C的基态原子核外电子排布式为
(3)B的基态原子中核外电子占据
(4)B、C、D三种元素的电负性由大到小的顺序是
(5)X与D原子结合形成的XD42-离子的中心原子杂化类型为
(6)W元素的基态原子价电子排布为
(7)化合物EA与水反应时,有气体生成,该化学反应方程式为
(8)化合物B3C4晶体中,元素B的化合价为
(9)元素X、Z、B、C所形成的Z(XBC)3是配合物,若中心原子与配位离子主要是以1:1的个数比配合所得离子显血红色,则该配合物的配离子化学式为
A.离子键 B.极性键 C.非极性键 D.配位键.
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为
(3)COCl2俗称光气,分子中C原子采取
(4)①短周期某主族元素M的逐级电离能情况如下图A所示,则M元素形成化合物时表现的主要化合价为
②第三周期8种元素按单质熔点高低的顺序如下图B所示,其中序号“8”代表
(5)由C原子跟Si原子以1:1相互交替结合而形成的晶体,晶型与晶体Si相同.两者相比熔点更高的是
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是

(2)二氧化钛作光催化剂能将居室污染物甲醛、苯、二甲苯等有害物质可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二甲苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体,分子中原子共平面,且都有三种二氯代物;
B.二氧化碳、甲醛、氯仿(CHCl3)中碳原子分别采用sp、sp2、sp3杂化;
C.对二甲苯是非极性分子,邻二甲苯和间二甲苯都是极性分子;
D.氨比甲醛易溶于水,是因为甲醛与水分子间不能形成氢键.
(3)日常生活中广泛使用的不锈钢就是含铬合金,铬元素原子中末成对电子数为
(4)①短周期某主族元素M的逐级电离能情况如下图A所示,则M元素形成化合物时,表现的主要化合价为
②第三周期八种元素按单质熔点高低的顺序如下图B所示,其中序号“8”代表

(5)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.科学家把C60和K掺杂在一起制造了一种富勒烯
 化合
化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质的K原子和C60分子的个数比为
(6)在配合物Fe(SCN)2+离子中,提供空轨道接受孤对电子的微粒是
(16分)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料。已知CuSO4·5H2O的部分结构可表示如下: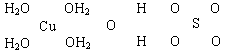
(1)写出铜原子价电子层的电子排布式____________,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有__________(填元素符号)。
(2)请在上图中把CuSO4·5H2O结构中的化学键用短线“——”表示出来。
(3)往浓CuSO4溶液中加入过量较浓的NH3·H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液。小心加入约和溶液等体积的C2H5OH并使之分成两层,静置。经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是______________________________________________。
(4)Cu(NH3)4SO4·H2O晶体中呈正四面体的原子团是______________,杂化轨道类型是sp3的原子是____________________________。
(5)如将深蓝色溶液加热,可能得到什么结果?________________________________。
(6)把CoCl2溶解于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+。此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的化学式(钴的配位数为6)___________,此配合物中的Co化合价为__ ____。