摘要:浓度为0.5moL·L-1的盐酸VL.欲使其浓度增大一倍.下列采取的方法正确的是( ) A.加入0.125VL 5moL·L-1的盐酸 B.通入标准状况下的HCl气体11.2L C.溶液加热浓缩至0.5VL D.加入10moL·L-1的盐酸0.1VL.再将溶液稀释至1.5VL.
网址:http://m.1010jiajiao.com/timu3_id_360508[举报]
欲用18mol/L的浓硫酸(密度为1.84g/mL)配制成浓度为 0.5mol/L 的稀硫酸 500mL.
(1)选用的主要仪器有:烧杯、量筒、胶头滴管、玻璃棒和
(2)请将下列各操作按正确的序号填写在横线上
(3)简要回答下列问题:①所需浓硫酸的体积为
查看习题详情和答案>>
(1)选用的主要仪器有:烧杯、量筒、胶头滴管、玻璃棒和
500ml容量瓶
500ml容量瓶
.(2)请将下列各操作按正确的序号填写在横线上
AEFCBD
AEFCBD
.A.用量筒量取浓硫酸 B.反复颠倒摇匀 C.用胶头滴管加水至刻度D.将配制好的溶液转入试剂瓶中贴上标签E.稀释浓硫酸F.将溶液转入容量瓶(3)简要回答下列问题:①所需浓硫酸的体积为
13.9
13.9
mL;②如果实验室有15mL、20mL、50mL的量筒,应选用15
15
mL.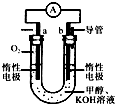 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.(1)工业生产甲醇的常用方法是CO(g)+2H2(g)?CH3OH(g);△H=-90.8kJ?mol-1.
已知:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1;
H2(g)+
| 1 | 2 |
2CO(g)+O2(g)═2CO2(g);△H=-566.0kJ?mol-1;
CH3OH(g)═CH3OH(l);△H=-37.3kJ?mol-1.
①计算液体CH3OH的燃烧热为
-1453/mol
-1453/mol
.②若在恒温恒容的容器内进行反应CO(g)+2H2(g)?CH3OH(g),下列表示该反应达到平衡状态的标志有
BC
BC
(填字母).A.有1个HH键生成的同时有3个CH键生成
B.CO百分含量保持不变
C.容器中混合气体的压强不变化
D.容器中混合气体的密度不变化
(2)制甲醇所需要的H2,可用下列反应制取:H2O(g)+CO(g)?H2(g)+CO2(g);△H<0.某温度下该反应的平衡常数K=1,若起始时c(CO)=1mol?L-1,c(H2O)=2mol?L-1,试回答下列问题:
①该温度下,反应进行一段时间后,测得H2的浓度为0.5mol?L-1,则此时该反应v(正)
>
>
(填“>”“<”或“=”)v(逆).②若反应温度不变,达到平衡后,H2O的转化率为
33.3%
33.3%
.(3)某实验小组设计了如图所示的甲醇燃料电池装置.
①该电池工作时,OH-向
b
b
(填“a”或“b”)极移动.②工作一段时间后,测得溶液的pH减小,该电池负极反应的电极反应式为
CH3OH+8OH--6e-=CO32-+6H2O
CH3OH+8OH--6e-=CO32-+6H2O
. A、B、C、X是中学化学1中常见的4种物质,它们均由短周期元素组成,转化关系如图所示.请针对以下两种情况1回答下列问题:
A、B、C、X是中学化学1中常见的4种物质,它们均由短周期元素组成,转化关系如图所示.请针对以下两种情况1回答下列问题:(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在.将A、C的水溶液混合可得白色胶状沉淀B.
①A中含有的金属元素为
铝
铝
(填元素名称).②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,此反应的化学方程式为
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
.
| ||
(2)若A、B、C的焰色反应均呈黄色,水溶液均呈碱性.
①A中所含有的化学键是
离子键
离子键
、共价键
共价键
.②将4.48L(标准状况下)X通入100mL 3mol?L-1A的水溶液后,溶液中离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.③自然界中存在由B或C与H2O按一定比例结晶而成的固体.将一定量的由C与H2O按一定比例形成的晶体溶于水配制成100mL溶液,测得溶液中金属阳离子的浓度为0.5mol?L-1.若取相同质量的此晶体加热至恒重,剩余固体的质量为
2.65g
2.65g
.