摘要:5.(2)g.c.d.a.b.e.f.h (3)上,燃着的木条放在烧瓶口上方.火焰熄灭说明CO2已充满 ②偏低:CO2气体中杂质气体H2S.HCl.H2O(g)比CO2分子量小 解析:(1)w1应为烧瓶.橡皮塞以及瓶内空气的质量. (2)用装置F制取CO2气体.并分别经过装置D.C.E以除去HCl.H2S以及水蒸气等杂质.最后在烧瓶A中收集. (3)CO2比空气重.故用向上排气法收集.检验CO2的方法通常是使燃着的木条熄灭的方法,w2为CO2气体.橡皮塞.烧瓶的总质量. (4)V为收集的CO2的体积.
网址:http://m.1010jiajiao.com/timu3_id_360214[举报]
A、B、C、D、E、F、G、H、I、J分别代表十种不同的有机物(其中A是化学工业重要原料之一).它们之间的相互转化关系如图: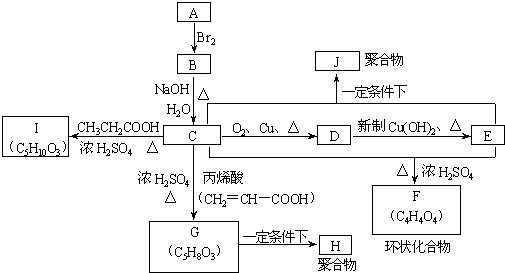
请回答下列问题:
(1)A的结构式简为
 ;指G→H的反应类型
;指G→H的反应类型
(2)写出下列转化的化学方程式.
①C→I
②C+E→J
(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
查看习题详情和答案>>

请回答下列问题:
(1)A的结构式简为
CH2=CH2
CH2=CH2
;F的结构简式为

加聚反应
加聚反应
.(2)写出下列转化的化学方程式.
①C→I
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
CH3CH2COOH+HOCH2CH2OH
CH3CH2COOCH2CH2OH+H2O
| 浓硫酸 |
| △ |
②C+E→J
nCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2OnCH2OHCH2CH2OH+nHOOCCOOH
 +(2n-1)H2O
+(2n-1)H2O
| 催化剂 |
 +(2n-1)H2O
+(2n-1)H2O(3)G有多种同分异构体,其中能与NaOH溶液及硫酸溶液均可反应;能发生银镜反应且生成的银与相应有机物的物质的量比为4:1,由符合条件的同分异构体数目有
5
5
种,写出其中的一种同分异构体结构简式HCOOCH2CH2CH2CHO
HCOOCH2CH2CH2CHO
.A、B、C、D、E、F、G七种短周期元素的原子序数依次增大.A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y );D形成的分子为单原子分子.回答问题:
(1)D元素的名称为
 .
.
(2)写出液态化合物Y的一种用途
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式:
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B2和液态X,并放出408.8kJ热量.查资料可知:
2Y(1)=2X(1)+C2(g)△H=-196.4kJ?mol-1写出液态W与气态C2反应生成液态X和气态B2的热化学方程式为
(6)G为氯,以K2CrO4为指示剂,用标准硝酸银溶液可以测定溶液中Cl-的浓度,已知Ksp(AgCl)=1.56ⅹ10-10,Ksp(Ag2CrO4)=1.10ⅹ10-12,Ag2CrO4为砖红色,则滴定终点的现象是
查看习题详情和答案>>
(1)D元素的名称为
氖
氖
,F形成的离子的结构示意图为

(2)写出液态化合物Y的一种用途
一定浓度的H2O2溶液作消毒剂
一定浓度的H2O2溶液作消毒剂
.(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,使用这种气球存在的隐患是易燃、易爆
易燃、易爆
.(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式:
H++HSO3-=H2O+SO2↑
H++HSO3-=H2O+SO2↑
.(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B2和液态X,并放出408.8kJ热量.查资料可知:
2Y(1)=2X(1)+C2(g)△H=-196.4kJ?mol-1写出液态W与气态C2反应生成液态X和气态B2的热化学方程式为
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1
.该反应还可设计为原电池(以KOH溶液为电解质溶液),请写出该电池的负极反应式:N2H4-4e-+4OH-=N2+4H2O
N2H4-4e-+4OH-=N2+4H2O
.(6)G为氯,以K2CrO4为指示剂,用标准硝酸银溶液可以测定溶液中Cl-的浓度,已知Ksp(AgCl)=1.56ⅹ10-10,Ksp(Ag2CrO4)=1.10ⅹ10-12,Ag2CrO4为砖红色,则滴定终点的现象是
滴入最后一滴硝酸银溶液时,溶液中出现砖红色深沉,振荡后砖红色沉淀不溶解
滴入最后一滴硝酸银溶液时,溶液中出现砖红色深沉,振荡后砖红色沉淀不溶解
.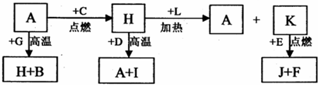 A、B、C、D、E、F 是常见单质,其中 A 是用量最大,应用最广泛的金属;元素 D 是地壳中含量最多的金属元素:D 元素和 E 元素在周期表中相邻,G、H、l、J、K、L 是常见化合物,其中 G 在常温下是无色液体,H 是黑色晶体,以上物质相互间的转化关系如图所示:
A、B、C、D、E、F 是常见单质,其中 A 是用量最大,应用最广泛的金属;元素 D 是地壳中含量最多的金属元素:D 元素和 E 元素在周期表中相邻,G、H、l、J、K、L 是常见化合物,其中 G 在常温下是无色液体,H 是黑色晶体,以上物质相互间的转化关系如图所示:请回答下列问题:
(1)元素 A 在元素周期表中的位置为
四
四
(周期)VIII
VIII
(族).(2)写出 K 的电子式
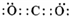
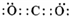
(3)写出 H 和 D 反应的化学方程式
3Fe3O4+8Al
4A12O3+9Fe
| ||
3Fe3O4+8Al
4A12O3+9Fe
.
| ||
(4)D 能与氢氧化钠溶液反应,请写出该反应的离子方程式:
3Fe3O4+8Al
4A12O3+9Fe;
| ||
3Fe3O4+8Al
4A12O3+9Fe;
.
| ||
(5)写出 A 与 G 反应的化学方程式
3Fe+4H2O ( g )
Fe3O4+4H2
| ||
3Fe+4H2O ( g )
Fe3O4+4H2
.
| ||
(6)K 与 E 反应时产生的现象有
镁带剧烈燃烧,(产生耀眼的白光,)瓶壁或瓶底出现白色固体和黑色颗粒
镁带剧烈燃烧,(产生耀眼的白光,)瓶壁或瓶底出现白色固体和黑色颗粒
,该反应的化学方程式为2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
A、B、C、D、E、F属于短周期主族元素.A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零,C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差.
(1)离子B-的结构示意图为
 ;化合物CE2的分子属于
;化合物CE2的分子属于
 .
.
(2)A、E、F形成的简单离子的半径由大到小的顺序为
(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
查看习题详情和答案>>
(1)离子B-的结构示意图为


非极性
非极性
分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程

(2)A、E、F形成的简单离子的半径由大到小的顺序为
S2->O2->Na+
S2->O2->Na+
(用离子符号表示);元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)金刚石(石墨)>晶体硅>氧气
金刚石(石墨)>晶体硅>氧气
.(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
.(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
C4H10+13O2--26e-=4CO2+5H2O
C4H10+13O2--26e-=4CO2+5H2O
,电池工作时,电解质里的CO32-向负
负
极移动.