摘要:已知短周期元素X和Y形成的常见离子化合物的化学式是Y2X.Y2X2.则这两种元素的原子序数之和为 A.9 B.17 C.18 D.19 8.可逆反应:aA+dD中.A 和C都为无色气体.达平衡后.有关叙述正确的是 A.若添加B.再达平衡.体系颜色加深.则B必为气体 B.增大压强.平衡不移动.则a+b一定等于c+d C.若升温.A的转化率降低.说明逆反应是吸热反应 D.若B为气体.则加入A.使A.B的转化率均得到提高
网址:http://m.1010jiajiao.com/timu3_id_360080[举报]
短周期元素X.Y.Z.W及生活中常见金属K,已知X原子的L层比Y原子的L层少3个电子,Y原子的最外层电子数跟X原子的核电荷数相等.Z元素的原子序数等于该元素原子的最外层电子数,K的高价氯化物形成的盐溶液,常用于印刷电路板电路的“刻蚀”.
试回答下列问题:(1)X是 ,Y是 .(填元素符号)
(2)Z分别与X.Y形成的化合物A.B均可用如图的装置制取和收集,则:
①制取纯净的气体A时分液漏斗中加入 ,制取和收集干燥的气体A时仪器接口顺序为 .
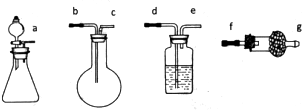
②A与B反应生成物C,通过加热C能否得到纯净得A .(填“能”或“不能”)
③该装置是否能制取Y的单质 (填“能”或“不能”),若能,则反应得离子方程式(若不能则此空不填) .
(3)W的单质可分别在X、Y的单质中燃烧,生成化合物C和D,C与水反应生成白色沉淀和化合物A,W的名称 .
(4)K在周期表中的位置为 ,现由含lmolHNO3溶质的稀硝酸与一定量的K恰好完全反应,稀硝酸的还原产物只有NO,则生成标准状况下NO的体积为 升.
查看习题详情和答案>>
试回答下列问题:(1)X是
(2)Z分别与X.Y形成的化合物A.B均可用如图的装置制取和收集,则:
①制取纯净的气体A时分液漏斗中加入

②A与B反应生成物C,通过加热C能否得到纯净得A
③该装置是否能制取Y的单质
(3)W的单质可分别在X、Y的单质中燃烧,生成化合物C和D,C与水反应生成白色沉淀和化合物A,W的名称
(4)K在周期表中的位置为
短周期元素X、Y、Z在周期表中的位置如图所示,已知X与Y的质子数之和等于Z的质子数,下列说法正确的是( )
| X | Y |
| Z |
| A、第一电离能:X<Y |
| B、X单质的化学性质比Z单质活泼 |
| C、X与Y可形成多种化合物,其中XY2分子间存在氢键 |
| D、X的常见氢化物的稳定性比Z的氢化物强 |
已知短周期的主族元素X、Y、Z、W、M的原子序数依次增大,X 是常见化肥的主要元素,Y 原子的最外层只有2个电子,Z单质可制成半导体材料,W元素形成的单质为黄色的固体.请回答以下问题:
(1)元素W在周期表的位置为 ;
(2)X与Y形成的化合物的电子式 ;
(3)Z的氧化物晶体类型为 ,12gZ的氧化物中含有的共价键数为 ;
(4)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为 ;
(5)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱 (用方程式书写或文字说明).
查看习题详情和答案>>
(1)元素W在周期表的位置为
(2)X与Y形成的化合物的电子式
(3)Z的氧化物晶体类型为
(4)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为
(5)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱
(13分)已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素。
(1)W在周期表中的位置: 。
(2)在一定条件下,容积为1L密闭容器中加入1.2molX2和0.4molY2,发生如下反应:
3X2 (g) + Y2(g)  2YX3(g) △H
2YX3(g) △H
反应各物质的量浓度随时间变化如下:
①计算该温度下此反应的平衡常数K= 。
②若升高温度平衡常数K减小,则△H 0(填“>”、“<”或“=”)。
③改变下列条件,能使该平衡向正反应方向移动且平衡常数不变的是 (填字母)。
a.增大压强 b. 降低温度 c.使用催化剂 d. 增大反应物的浓度
(3)常见液态化合物X2Z2的稀溶液易被催化分解,可使用的催化剂为 (填字母)。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)A是四种元素中三种元素组成的电解质,溶液呈碱性,将常温下0.1mol·L-1的A溶液稀释至原体积的10倍后溶液的pH=12,则A的电子式为 。
(5)以X2为燃料可制成燃料电池。已知:2X2(g)+Z2(g)=2X2Z(l) △H=?572KJ·mol-1
该燃料电池释放228.8KJ电能时,生成1mol液态X2Z,该电池的能量转化率为 。