摘要:D 22.A
网址:http://m.1010jiajiao.com/timu3_id_359825[举报]
22 A、B是两种钠盐,且都是正盐,A中含有两种元素,B中含有三种元素,C是一种常 见的二元强酸,且A、B、C中皆含有同一元素,D有臭鸡蛋气味,它们在水溶液中有如下转化关系:www..com
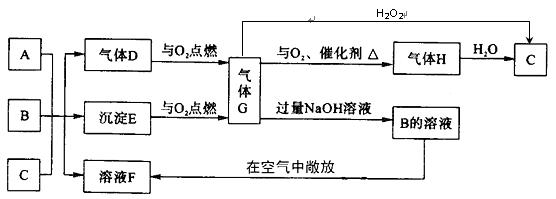
试回答:
(1)A、D、G的化学式分别为 、 、 ![]() [来源:Zxxk.Com]
[来源:Zxxk.Com]
(2)A、B、C反应只生成E和F的离子方程式为 。
(3)要发生上述转化,A、B物质的量之比![]() 应满足的关系是 。
应满足的关系是 。
(4)气体G可使高锰酸钾溶液褪色,发生反应的离子方程式为 。
查看习题详情和答案>>A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2.C、D的电离能数据如下(kJ?mol-1):
(1)化合价是元素的一种性质.由C、D的电离能数据判断,C通常显
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供
(5)如图所示晶胞中,阳离子与阴离子的个数为
查看习题详情和答案>>
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
+2
+2
价,D显+3
+3
价;(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
1
1
个σ键,2
2
个π键;(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
.| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供空轨道
空轨道
,AB提供孤对电子
孤对电子
.(5)如图所示晶胞中,阳离子与阴离子的个数为
3:1
3:1
.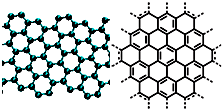 A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:
A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:(1)下列有关石墨烯说法正确的是
BD
BD
.A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合.
①钴原子在基态时,核外电子排布式为:
[Ar]3d74s2
[Ar]3d74s2
.
②乙醇沸点比氯乙烷高,主要原因是
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
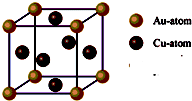
.③右图是金与铜形成的金属互化物合金,它的化学式可表示为:
Cu3Au或AuCu3
Cu3Au或AuCu3
.④含碳源中属于非极性分子的是
a、b、c
a、b、c
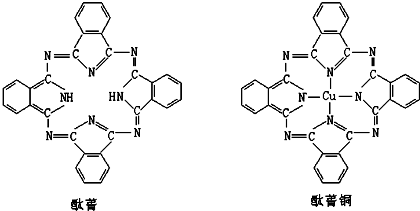
(a.甲烷 b.乙炔 c.苯 d.乙醇)⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:
sp3和sp2
sp3和sp2
;酞菁铜分子中心离子的配位数为:2
2
.
B.硫酸钾是重要的化工产品,生产方法很多,如曼海姆法、石膏两步转化法等.
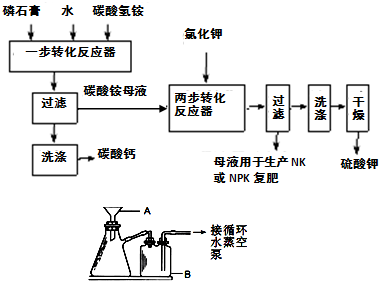
(1)本实验中,采用抽滤方法,图中A、B两仪器名称分别为:
布氏漏斗
布氏漏斗
、安全瓶
安全瓶
.(2)在一部转化反应器中发生的反应为:CaSO4?2H2O+2NH4HCO3=(NH4)2SO4+CaCO3+CO2↑+3H2O,该步反应温度必须低于35℃,其主要目的是
防止NH4HCO3分解
防止NH4HCO3分解
无此空
无此空
.(3)在两步转化反应器中发生反应的化学方程式为
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
无此空
无此空
.(4)两步转化反应器中用乙二醇代替水作溶剂,其目的是
降低K2SO4溶解度
降低K2SO4溶解度
有利于K2SO4析出,提高产率
有利于K2SO4析出,提高产率
.(5)磷石膏主要成分为二水硫酸钙(CaSO4?2H2O),还含有未分解的磷矿,未洗涤干净的磷酸、氟化钙、铁铝氧化物等,欲检验母液中含Fe3+,可用亚铁氰化钾溶液检验,该检验反应的离子方程式为:
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
.(6)该法优点除K2SO4产率高外,再列举一个优点
原料得到充分利用
原料得到充分利用
同时得到副产品化肥等
同时得到副产品化肥等
.A、B、C、D四种元素处于同一周期.在同族元素中,A的气态氢化物沸点最高,B的最高价氧化物对应水化物的酸性在同周期中最强,C的电负性介于A、B之间,D与B相邻.
(1)C原子的价电子排布式为
(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)
(3)B的单质分子中存在
(4)A的气态氢化物的沸点在同族中最高的原因
查看习题详情和答案>>
(1)C原子的价电子排布式为
2s22p4
2s22p4
.(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)
F>N>O
F>N>O
.(3)B的单质分子中存在
2
2
个π键;B的气态氢化物BH3分子中的中心原子轨道采用sp3
sp3
杂化.B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于原子
原子
晶体,其硬度比金刚石大
大
(填“大”或“小”).(4)A的气态氢化物的沸点在同族中最高的原因
HF分子之间可以形成氢键从而使沸点升高
HF分子之间可以形成氢键从而使沸点升高
.A、B、C、D、E 5种短周期元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C;C、E 同主族.
(1)B在周期表中的位置第
(2)C、E 两种元素可能形成化合物的化学式
(3)化合物BC与C2反应的化学方程式
(4)1.6gB2A4液体与C2气体反应生成B2气体和液态A2C,放出31.05kJ的热量,写出1molB2A4反应的热化学方程式:
查看习题详情和答案>>
(1)B在周期表中的位置第
2
2
周期,第ⅤA
ⅤA
族;(2)C、E 两种元素可能形成化合物的化学式
SO2或SO3
SO2或SO3
;(3)化合物BC与C2反应的化学方程式
2NO+O2=2NO2
2NO+O2=2NO2
;(4)1.6gB2A4液体与C2气体反应生成B2气体和液态A2C,放出31.05kJ的热量,写出1molB2A4反应的热化学方程式:
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-621.0kJ?mol-1
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-621.0kJ?mol-1
.