摘要:14.用铂电极电解NaCl和CuSO4的混合溶液.当电路中通过4mol电子电量时.阴.阳两极都产生1.4mol气体.电解后溶液体积为4L.则最后电解液的pH值最接近 A.4 B.2 C.13 D.14
网址:http://m.1010jiajiao.com/timu3_id_357538[举报]
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.戊为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1.

(1)足量的M溶液可能是
A.AgNO3溶液 B.NaOH溶液 C.HCl溶液 D.NaCl溶液 E.CuSO4溶液 F.Na2SO4溶液
(2)丙的现象
(3)电解一段时间后乙溶液观察到的现象
(4)丁中
(5)下列说法正确的是
A.继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,各电解池均将恢复原状.
B.如图电解过程M中A极附近的pH一定增大
C.将氯化钠固体溶于酒精中可以形成与丁中相同的分散系.
查看习题详情和答案>>

(1)足量的M溶液可能是
BF
BF
(填序号).A.AgNO3溶液 B.NaOH溶液 C.HCl溶液 D.NaCl溶液 E.CuSO4溶液 F.Na2SO4溶液
(2)丙的现象
n端变红,m端出现蓝色
n端变红,m端出现蓝色
.(3)电解一段时间后乙溶液观察到的现象
有白色浑浊产生
有白色浑浊产生
.某同学认为在D极会有两种气体产生,写出反应过程中的方程式:2H2O
2H2↑+O2↑,H20+CO32-=CO2↑+2OH-
| ||
2H2O
2H2↑+O2↑,H20+CO32-=CO2↑+2OH-
.
| ||
(4)丁中
E
E
(填“E”或“F”)极颜色加深,此移动的物质在过程中否
否
(填“是”或“否”)发生了化学变化.(5)下列说法正确的是
BC
BC
.A.继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,各电解池均将恢复原状.
B.如图电解过程M中A极附近的pH一定增大
C.将氯化钠固体溶于酒精中可以形成与丁中相同的分散系.
 如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹。丁为直流电源,x、y为电源的两极。G为电流计,电极均为石墨电极。闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹。丁为直流电源,x、y为电源的两极。G为电流计,电极均为石墨电极。闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:
(1)M溶液可能是 (填序号)。
A.KNO3溶液 B. Ba(OH)2溶液 C.H2SO4溶液
D. NaCl溶液 E.CuSO4溶液
(2)X为电源 极,m点的现象 。
(3)C极的电极反应式为 。
(4)若乙池中AgNO3溶液电解后体积为100mL,测得溶 液的pH=1, 则乙池中C极析出的固体质量为 g。
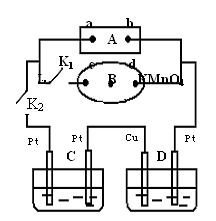 (5)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,且电流计G指针发生偏转,则A极电极反应式为 。
(5)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,且电流计G指针发生偏转,则A极电极反应式为 。
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.戊为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1.

(1)足量的M溶液可能是______(填序号).
A.AgNO3溶液 B.NaOH溶液 C.HCl溶液 D.NaCl溶液 E.CuSO4溶液 F.Na2SO4溶液
(2)丙的现象______.
(3)电解一段时间后乙溶液观察到的现象______.某同学认为在D极会有两种气体产生,写出反应过程中的方程式:
______ 2H2↑+O2↑,H20+CO32-=CO2↑+2OH- 查看习题详情和答案>>

(1)足量的M溶液可能是______(填序号).
A.AgNO3溶液 B.NaOH溶液 C.HCl溶液 D.NaCl溶液 E.CuSO4溶液 F.Na2SO4溶液
(2)丙的现象______.
(3)电解一段时间后乙溶液观察到的现象______.某同学认为在D极会有两种气体产生,写出反应过程中的方程式:
______ 2H2↑+O2↑,H20+CO32-=CO2↑+2OH- 查看习题详情和答案>>
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹。丁为直流电源,x、y为电源的两极。G为电流计,电极均为石墨电极。闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:
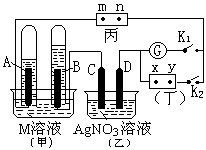
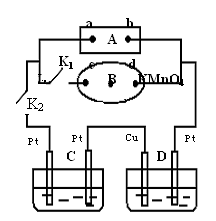
(1)M溶液可能是 (填序号)。
A.KNO3溶液 B. Ba(OH)2溶液 C.H2SO4溶液
D. NaCl溶液 E.CuSO4溶液
(2)X为电源 极,m点的现象 。
(3)C极的电极反应式为 。
(4)若乙池中AgNO3溶液电解后体积为100mL,测得溶 液的pH=1, 则乙池中C极析出的固体质量为 g。
(5)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,且电流计G指针发生偏转,则A极电极反应式为 。


(1)M溶液可能是 (填序号)。
A.KNO3溶液 B. Ba(OH)2溶液 C.H2SO4溶液
D. NaCl溶液 E.CuSO4溶液
(2)X为电源 极,m点的现象 。
(3)C极的电极反应式为 。
(4)若乙池中AgNO3溶液电解后体积为100mL,测得溶 液的pH=1, 则乙池中C极析出的固体质量为 g。
(5)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1,断开K2,发现A、B极的管内气体体积减少,且电流计G指针发生偏转,则A极电极反应式为 。
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.
(1)铁元素在元素周期表中的位置是______.
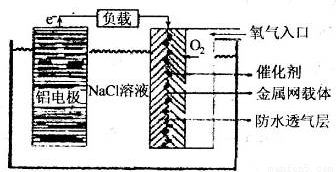
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为______;
②电池中NaCl的作用是______.
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为______,此时向溶液中加入8g CuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为______L.
(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______ 2AlCl3+3CO.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)铁元素在元素周期表中的位置是______.
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为______;
②电池中NaCl的作用是______.
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为______,此时向溶液中加入8g CuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为______L.
(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______ 2AlCl3+3CO.
 查看习题详情和答案>>
查看习题详情和答案>>