摘要:1]9 B 20 新戊烷 21 CH3CH3 22 2-甲基丁烷 23 2 4 5 24 CH4 CH2 CH3 CH 25 CH3COONa+NaOHCH4↑+Na2CO3 CH4O CH3OH 26 2-甲基-1-丁烯 2-甲基-2-丁烯 3-甲基-1-丁烯 27 2-甲基-5-乙基辛烷 (3)3,3,6-三甲基辛烷 (4)聚2,3-二甲基-1,3-戊二烯 (5)4,6,6-三甲基-1,4-庚二烯 (6)3-甲基-2-乙基-1-丁烯 28 ①和③.②和⑥ ⑦和⑧ ③和④ 29 CH3-CH=CH-CH2-CH=CH2(不能是CH3-CH2-CH=CH-CH=CH2.想想看.为什么?) 30 3,3-二甲基-2-乙基-1-丁烯.3,4,4-三甲基-2-戊烯.3,4,4-三甲基-1-戊烯 31 A是乙炔.B是乙烯.C是1,3-丁二烯.D是甲烷.E是环丙烷 32原混和气体由乙烷和甲烷组成.甲烷的体积为0.896升.乙烷的体积为0.448升. 33甲烷的体积为40毫升.氧气为70毫升. 34C2H6占66.7% C4H8占50% C4H10占40% 35(1)0 x-2y y-0.5x (2)C3H4 C3H6 C3H8
网址:http://m.1010jiajiao.com/timu3_id_356777[举报]
(2009?江门一模)(1)下表为某温度和压强下,密闭容器中SO2氧化为SO3反应在不同时间各物质的浓度(mol/L)
试画出V(SO3)-t图.
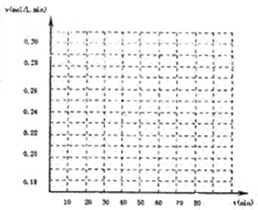
(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
①如何利用表中数据推断SO2的氧化反应的热效应?
②在400一500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:
③工业制硫酸所产生的尾气含有SO2、微量的SO3和酸雾.为了保护环境将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:
④能用于测定硫酸尾气中SO2含量的是
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
⑤某温度下,SO2氧化为SO3在10L的密闭容器中进行,开始向容器加入4.0mol SO2和10.0molO2,当反应达到平衡时,混合气体为13.0mol,则SO2的转化率为
查看习题详情和答案>>
| 时间(min) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| SO2 | 10 | 7 | 5 | 3.5 | 2 | 1 | 1 | 1 |
| O2 | 5 | 3.5 | 2.5 | 1.75 | 1 | 0.5 | 0.5 | 0.5 |
| SO3 | 0 | 3 | 5 | 6.5 | 8 | 9 | 9 | 9 |

(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
| 压强/MPa 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
压强一定时,温度升高,二氧化硫的转化率减小,说明升温平衡向逆反应方向移动,所以二氧化硫的氧化反应为放热反应
压强一定时,温度升高,二氧化硫的转化率减小,说明升温平衡向逆反应方向移动,所以二氧化硫的氧化反应为放热反应
.②在400一500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:
从化学平衡移动条件分析应该采用低温高压.而根据表格中提供的数据发现,压强的增加引起SO2转化率的变化并不明显,反而增加成本,所以工业上直接采用常压
从化学平衡移动条件分析应该采用低温高压.而根据表格中提供的数据发现,压强的增加引起SO2转化率的变化并不明显,反而增加成本,所以工业上直接采用常压
.③工业制硫酸所产生的尾气含有SO2、微量的SO3和酸雾.为了保护环境将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:
2H2SO3+O2=2H2SO4 ;2NH4HSO3+O2=2NH4HSO4
2H2SO3+O2=2H2SO4 ;2NH4HSO3+O2=2NH4HSO4
.④能用于测定硫酸尾气中SO2含量的是
BC
BC
.(填字母)A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
⑤某温度下,SO2氧化为SO3在10L的密闭容器中进行,开始向容器加入4.0mol SO2和10.0molO2,当反应达到平衡时,混合气体为13.0mol,则SO2的转化率为
50%
50%
,该温度反应的平衡常数1.1L?mol-1
1.1L?mol-1
.某研究性学习小组根据侯德榜制碱法原理并参考下表有关物质溶解度(g/100g水)数据,以饱和NaCl溶液与研细的NH4HCO3为原料,设计实验经两步反应制备纯碱.
下列有关说法中,正确的是( )
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 35℃以上分解 | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| A、第一、二步反应的基本类型为化合反应、分解反应 |
| B、第一、二步反应之间的主要实验操作是过滤、洗涤 |
| C、第一步反应控制温度高于30℃目的是提高反应产率 |
| D、反应液加盐酸处理可使NaCl循环使用并回收NH4Cl |
在1.013×105Pa下,测得某些烷烃的沸点如下表.经分析下列选项正确的是( )
|
查看习题详情和答案>>
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.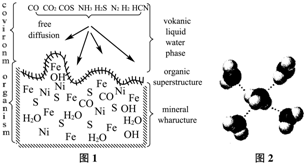
A.海底热液研究(图1)处于当今科研的前沿.海底热液活动区域“黑烟囱”的周围常存在FeS、黄铜矿及锌矿等矿物.
(1)Ni2+的核外电子排布式是
(2)分析下表,铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,基主要原因是
| 电离能/kJ?mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
A.电负性:N>O>S>C B.CO2与COS(硫化羰)互为等电子体
C.NH3分子中氮原子采用sp3杂化 D.CO、H2S、HCN都是极性分子
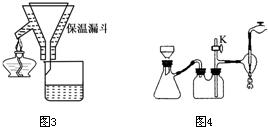
(4)“酸性热液”中大量存在一价阳离子,结构如图2,它的化学式为
(5)FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是
B.制备KNO3晶体的实质是利用结晶和重结晶法对KNO3和NaCl的混合物进行分离.下面是某化学兴趣小组的活动记录:
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
实验方案:
Ⅰ.溶解:称取29.8g KCl和34.0g NaNO3放入250mL烧杯中,再加入70.0g蒸馏水,加热并搅拌,使固体全部溶解.
Ⅱ.蒸发结晶:继续加热和搅拌,将溶液蒸发浓缩.在100℃时蒸发掉50.0g 水,维持该温度,在保温漏斗(如图3所示)中趁热过滤析出的晶体.得晶体m1g.
Ⅲ.冷却结晶:待溶液冷却至室温(实验时室温为10℃)后,进行减压过滤.得KNO3粗产品m2g.
Ⅳ.重结晶:将粗产品全部溶于水,制成100℃的饱和溶液,冷却至室温后抽滤.得KNO3纯品.
假定:①盐类共存时不影响各自的溶解度;②各种过滤操作过程中,溶剂的损耗忽略不计.试回答有关问题:
(1)操作Ⅱ中趁热过滤的目的是.
(2)若操作Ⅱ中承接滤液的烧杯中不加入蒸馏水,则理论上在操作Ⅲ中可得粗产品的质量m2=
(3)操作Ⅲ中采用减压过滤,其优点是