网址:http://m.1010jiajiao.com/timu3_id_356569[举报]
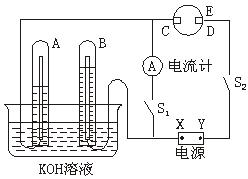
(1)标出电源的正、负极:X为____________极,Y为____________极。
(2)在滤纸的C端附近。观察到的现象是____________,在滤纸的D端附近,观察到的现象是____________。
(3)写电极反应式:A中____________;D中____________。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2,闭合开关S1,则电流计的指针是否发生偏转?(填“偏转”或“不偏转”)____________。
(5)若电流计指针偏转,写出有关的电极反应式(若指针“不偏转”,此题不必回答)____________。A中____________;B中____________。若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答)__________________。
查看习题详情和答案>>如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。
(3)写出电极反应式:B电极 。
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。

(10分)如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。?
(3)写出电极反应式:B电极 。?
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。?
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。?
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。
(10分)如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极。在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示。
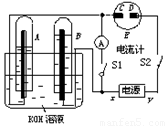
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。?
(3)写出电极反应式:B电极 。?
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。?
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。?
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。
查看习题详情和答案>>
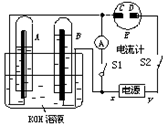
请回答下列问题:
(1)标出电源的正、负极:x为 。
(2)在滤纸的C端附近,观察到的现象是 。?
(3)写出电极反应式:B电极 。?
(4)若电解一段时间后,A、B中均有气体包围电极。此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转 (填“偏转”或“不偏转”)。?
(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答。);
。?
若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答) 。