摘要: D 2. B 3. D 4.A 5. C
网址:http://m.1010jiajiao.com/timu3_id_353348[举报]
A、B、C、D、E是原子序数依次增大的五种短周期元素,A的某种核素不含中子,B、E同主族,且E的L层电子数是K层和M层电子数之和,C是所有短周期元素中半径最大的元素、C、D、E三种元素的最高价氧化物对应水化物两两之间均可反应.试解答下列问题:
(1)B元素的简单离子的结构示意简图为
 .
.
(2)A、D、E元素的名称分别为
(3)E元素在周期表中的位置是第
(4)五种元素的简单离子半径从大到小的顺序是
(5)五种元素中,得电子能力最强的是
查看习题详情和答案>>
(1)B元素的简单离子的结构示意简图为


(2)A、D、E元素的名称分别为
氢
氢
、硫
硫
、铝
铝
.(3)E元素在周期表中的位置是第
三
三
周期ⅥA
ⅥA
族.(4)五种元素的简单离子半径从大到小的顺序是
S2->O2->Na+>Al3+>H+
S2->O2->Na+>Al3+>H+
(用元素离子符号填写).(5)五种元素中,得电子能力最强的是
O
O
,失电子能力最强的是Na
Na
(填元素符号). A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题:
(1)D的化学式为
H2
H2
.(2)反应③的离子方程式为
3NO2+H2O=2H++2NO3-+NO
3NO2+H2O=2H++2NO3-+NO
.(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
4NH3+6NO=5N2+6H2O
4NH3+6NO=5N2+6H2O
.(4)0.1mol?L-1的X溶液和0.1mol?L-1的Y溶液等体积混合,溶液呈
酸
酸
性(填“酸”、“碱”或“中”),原因是NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
(用离子方程式说明).(5)常温下0.1mol?L-1的Y溶液中c(H+)/c(OH-)=1×10-8,下列叙述正确的是
ACD
ACD
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度0.1mol?L-1
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol?L-1的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH为9.
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,Y的用量最大.相关物质间的关系如图所示.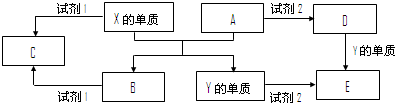
(1)X的单质与A反应的化学方程式是
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
②4.5克X的单质参加反应转移的电子数
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
查看习题详情和答案>>

(1)X的单质与A反应的化学方程式是
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
.
| ||
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
2Al+2H2O+2OH-═2AlO2-+3H2↑
2Al+2H2O+2OH-═2AlO2-+3H2↑
.②4.5克X的单质参加反应转移的电子数
3.01×1023
3.01×1023
.(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
.②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
.4-硫醚基喹唑啉类化合物是一种具有应用前景的抑菌药物,其合成路线如下:

已知:
(1)写出反应类型A→B
(2)满足下列条件的C的同分异构体的结构简式有
①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式
 .由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
.由C→D的反应中还可能生成一种有机副产物,该副产物的结构简式为
 .
.
(4)写出物质G的结构简式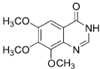
 .
.
(5)利用题给相关信息,以甲苯、HCONH2为原料,合成 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:① ; ②
; ② ;③
;③

 .
.
查看习题详情和答案>>

已知:

(1)写出反应类型A→B
取代反应
取代反应
,E→F还原反应
还原反应
.(2)满足下列条件的C的同分异构体的结构简式有
4
4
种(不包含C).①苯的衍生物,且苯环上的一取代产物有两种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含-COO-基团.
(3)写出C→D的化学方程式




(4)写出物质G的结构简式


(5)利用题给相关信息,以甲苯、HCONH2为原料,合成
 .合成过程中无机试剂任选;合成路线流程图示例为:
.合成过程中无机试剂任选;合成路线流程图示例为:
提示:①
 ; ②
; ② ;③
;③


A(C10H10O2)是生产某新型工程塑料的基础原料之一,A没有酸性,能使溴水褪色.A在酸性条件下水解生成有机物B和甲醇.
现拟从芳香烃 出发来合成A,合成路线如下:
出发来合成A,合成路线如下:
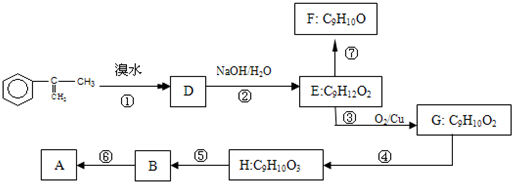
已知:烯醇结构不稳定,会自动异构化为醛:即R-CH=CH-OH→R-CH2-CHO.
(1)B中官能团的名称
(2)反应⑦属于消去反应
A加成反应 B消去反应 C氧化反应 D取代反应
(3)写出反应⑥的化学方程式: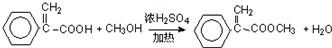

(4)反应⑦生成的有机物F有两种可能,结构简式分别为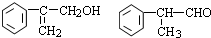
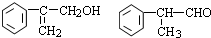 .
.
(5)①写出G与新制Cu(OH)2反应的方程式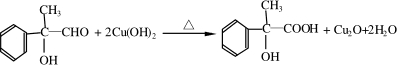

②与G互为同分异构体,能与NaHCO3溶液反应,且苯环上的一卤代物只有两种的G同分异构体有
(6)A在一定条件下能生成一种高分子化合物,写出该反应的化学方程式:
 .
.
查看习题详情和答案>>
现拟从芳香烃
 出发来合成A,合成路线如下:
出发来合成A,合成路线如下:
已知:烯醇结构不稳定,会自动异构化为醛:即R-CH=CH-OH→R-CH2-CHO.
(1)B中官能团的名称
羧基、碳碳双建
羧基、碳碳双建
(2)反应⑦属于消去反应
B
B
A加成反应 B消去反应 C氧化反应 D取代反应
(3)写出反应⑥的化学方程式:


(4)反应⑦生成的有机物F有两种可能,结构简式分别为
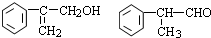
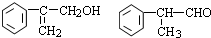
(5)①写出G与新制Cu(OH)2反应的方程式


②与G互为同分异构体,能与NaHCO3溶液反应,且苯环上的一卤代物只有两种的G同分异构体有
4
4
种.(6)A在一定条件下能生成一种高分子化合物,写出该反应的化学方程式:

