摘要:有4.8gCuO.Fe2O3混合物与充足的CO于加热时反应.充分反应后全部气体用
网址:http://m.1010jiajiao.com/timu3_id_351852[举报]
W、X、Y、Z是元素周期表前36号元素中的四种常见元素,其相关信息如下表:
(1)X单质在常温下与F2反应生成气态化合物XF4,该化合物晶体类型为 ;在加热或高温时X可与C12、Br2、I2反应生成XC14、XBr4、XI4.XC14的空间构型为 ,在X-F、X-Cl、X-Br、X-I四种共价键中,键能最小的是 .(用具体元素符号表示)
(2)Y位于元素周期表 区;Y在O2中燃烧产物与足量稀硝酸反应的离子方程式为 .
(3)Z+基态核外电子排布式为 ,ZCl2加热至773K分解为ZCl 的化学方程式为 .
(4)W的最高价氧化物与焦炭按物质的量1:3混合加热,生成CO2和化合物M,M的化学式为: .
查看习题详情和答案>>
| 元素 | 相关信息 |
| W | 最高价氧化物既能与强碱又能与强酸反应形成盐和水,又可作耐火材料 |
| X | 以化合态广泛存在于自然界,单质可用于制造集成电路 |
| Y | 基态原子核外有4个未成对电子 |
| Z | 其硫酸盐常用于检验或除去乙醇、乙醚等有机溶剂中的少量水分 |
(2)Y位于元素周期表
(3)Z+基态核外电子排布式为
(4)W的最高价氧化物与焦炭按物质的量1:3混合加热,生成CO2和化合物M,M的化学式为:
(2012?天津)萜品醇可作为消毒剂、抗氧化剂、医药和溶剂.合成a-萜品醇G的路线之一如下:
已知:RCOOC2H5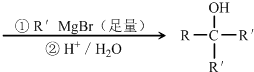
请回答下列问题:
(1)A所含官能团的名称是
(2)A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式:
 .
.
(3)B的分子式为
 .
.
①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
(4)B→C、E→F的反应类型分别为
(5)C→D的化学方程式为 +2NaOH
+2NaOH
 +NaBr+2H2O
+NaBr+2H2O +2NaOH
+2NaOH
 +NaBr+2H2O.
+NaBr+2H2O.
(6)试剂Y的结构简式为
(7)通过常温下的反应,区别E、F和G的试剂是
(8)G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式:
 .
.
查看习题详情和答案>>

已知:RCOOC2H5

请回答下列问题:
(1)A所含官能团的名称是
羰基、羧基
羰基、羧基
.(2)A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式:


(3)B的分子式为
C8H14O3
C8H14O3
;写出同时满足下列条件的B的链状同分异构体的结构简式:

①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
(4)B→C、E→F的反应类型分别为
取代反应
取代反应
、酯化反应
酯化反应
.(5)C→D的化学方程式为
 +2NaOH
+2NaOH
 +NaBr+2H2O
+NaBr+2H2O +2NaOH
+2NaOH
 +NaBr+2H2O
+NaBr+2H2O(6)试剂Y的结构简式为
CH3MgBr
CH3MgBr
.(7)通过常温下的反应,区别E、F和G的试剂是
Na
Na
和NaHCO3溶液
NaHCO3溶液
.(8)G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式:


(2012?唐山二模)图中,A~L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见的金属单质,E的稀溶液为蓝色,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味的气体,且能使品红溶液褪色.
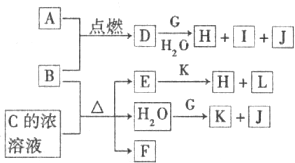
回答下列问题:
(1)A元素在周期表中的位置是
(2)①D的水溶液与G反应的离子方程式为
②A和K是重要的化工原料,工业上同时制取A单质和K的反应的化学方程式为
(3)若将标准状况下2.24L的F通入150mL 1.0m1?L-1的K溶液中,充分反应后,测得溶液显酸性,所得溶质及其物质的量分别为
(4)与F组成元素相同的一种-2价酸根离子M,M中两种元素的质量比为4:3,已知1mol A单质与含1mol M的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生.取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.则A单质与含M的溶液反应的离子方程式为
查看习题详情和答案>>

回答下列问题:
(1)A元素在周期表中的位置是
第3周期ⅦA族
第3周期ⅦA族
(填所在周期和族),K固体中所含的化学键有离子键和共价键(或极性共价键)
离子键和共价键(或极性共价键)
.(2)①D的水溶液与G反应的离子方程式为
Cu2++2H2O+2Na═Cu(OH)2↓+2Na++H2↑
Cu2++2H2O+2Na═Cu(OH)2↓+2Na++H2↑
.②A和K是重要的化工原料,工业上同时制取A单质和K的反应的化学方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(3)若将标准状况下2.24L的F通入150mL 1.0m1?L-1的K溶液中,充分反应后,测得溶液显酸性,所得溶质及其物质的量分别为
Na2SO3为0.05mol,NaHSO3为0.05mol
Na2SO3为0.05mol,NaHSO3为0.05mol
.(4)与F组成元素相同的一种-2价酸根离子M,M中两种元素的质量比为4:3,已知1mol A单质与含1mol M的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生.取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.则A单质与含M的溶液反应的离子方程式为
Cl2+S2O32-+H2O═2Cl-+2H++S↓+SO42-
Cl2+S2O32-+H2O═2Cl-+2H++S↓+SO42-
.普罗帕酮为广谱高效膜抑制性抗心律失常药.其合成路线如下:
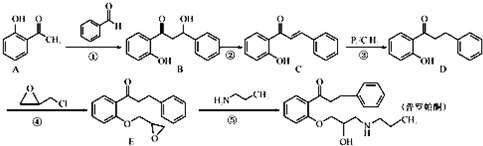
(1)化合物C的含氧官能团为 和 (填官能团的名称).
(2)反应①→④中属于加成反应的是 (填序号).
(3)写出同时满足下列条件的A的同分异构体结构简式: .
Ⅰ.分子中含有苯环,且苯环上的一氯代物有两种;
Ⅱ.与FeCl3溶液发生显色反应;
Ⅲ.能发生银镜反应.
(4)产物普罗帕酮中会混有少量副产物F(分子式为C21H27O3N).F的结构简式为 .
(5)化合物3羟基戊二酸二乙酯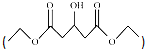 是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用) .合成路线流程图示例如下:
是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用) .合成路线流程图示例如下:
H2C═CH2
CH3CH2Br
CH3CH2OH.
查看习题详情和答案>>

(1)化合物C的含氧官能团为
(2)反应①→④中属于加成反应的是
(3)写出同时满足下列条件的A的同分异构体结构简式:
Ⅰ.分子中含有苯环,且苯环上的一氯代物有两种;
Ⅱ.与FeCl3溶液发生显色反应;
Ⅲ.能发生银镜反应.
(4)产物普罗帕酮中会混有少量副产物F(分子式为C21H27O3N).F的结构简式为
(5)化合物3羟基戊二酸二乙酯
 是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)
是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)H2C═CH2
| HBr |
| NaOH溶液 |
| △ |
某同学设计的制取氯气和验证氯气部分化学性质的实验装置如下图甲所示:

其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸,F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球.回答下列问题:
(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,请写出A处反应的离子方程式:
(2)B处饱和食盐水是为了除去
(3)实验中可观察到颜色的变化:D处
(4)当F处棉球变色,立即关闭活塞K,可看到I瓶中液面上升,H瓶中充满黄绿色气体,则H瓶中加入的液体一般为
查看习题详情和答案>>

其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸,F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球.回答下列问题:
(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,请写出A处反应的离子方程式:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
(2)B处饱和食盐水是为了除去
HCl
HCl
,C处浓硫酸的作用是干燥氯气
干燥氯气
.(3)实验中可观察到颜色的变化:D处
不变色
不变色
,E处先变红,后褪色
先变红,后褪色
,F处变蓝
变蓝
,G处棉球的作用是吸收多余的氯气
吸收多余的氯气
,G处反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.(4)当F处棉球变色,立即关闭活塞K,可看到I瓶中液面上升,H瓶中充满黄绿色气体,则H瓶中加入的液体一般为
饱和食盐水
饱和食盐水
;甲中H-I装置的作用为收集氯气
收集氯气
.若将甲中的H-I装置置换为乙装置,是否可行(填“是”或“否”)否
否
,理由是密闭装置,气体压力大时易爆炸
密闭装置,气体压力大时易爆炸
.