��Ŀ����
��2012?��ɽ��ģ��ͼ�У�A��LΪ�������ʻ�����ʵ�ˮ��Һ��B��A������ȼ�ղ����ػ�ɫ�̣�B��GΪ��ѧ��ѧ�г����Ľ������ʣ�E��ϡ��ҺΪ��ɫ��I����ɫ��ӦΪ��ɫ�����J��Ԫ��ԭ�Ӻ���ֻ��һ�����ӣ�FΪ��ɫ���д̼�����ζ�����壬����ʹƷ����Һ��ɫ��
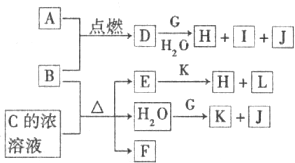
�ش��������⣺
��1��AԪ�������ڱ��е�λ����
��2����D��ˮ��Һ��G��Ӧ�����ӷ���ʽΪ
��A��K����Ҫ�Ļ���ԭ�ϣ���ҵ��ͬʱ��ȡA���ʺ�K�ķ�Ӧ�Ļ�ѧ����ʽΪ
��3��������״����2.24L��Fͨ��150mL 1.0m1?L-1��K��Һ�У���ַ�Ӧ�����Һ�����ԣ��������ʼ������ʵ����ֱ�Ϊ
��4����F���Ԫ����ͬ��һ��-2���������M��M������Ԫ�ص�������Ϊ4��3����֪1mol A�����뺬1mol M����Һ��ǡ����ȫ��Ӧ����Ӧʱ���۲쵽��dz��ɫ����������ȡ��Ӧ����ϲ���Һ���������ữ���Ȼ�����Һ���а�ɫ������������A�����뺬M����Һ��Ӧ�����ӷ���ʽΪ

�ش��������⣺
��1��AԪ�������ڱ��е�λ����
��3���ڢ�A��
��3���ڢ�A��
�����������ں��壩��K�����������Ļ�ѧ�������Ӽ����ۼ������Թ��ۼ���
���Ӽ����ۼ������Թ��ۼ���
����2����D��ˮ��Һ��G��Ӧ�����ӷ���ʽΪ
Cu2++2H2O+2Na�TCu��OH��2��+2Na++H2��
Cu2++2H2O+2Na�TCu��OH��2��+2Na++H2��
����A��K����Ҫ�Ļ���ԭ�ϣ���ҵ��ͬʱ��ȡA���ʺ�K�ķ�Ӧ�Ļ�ѧ����ʽΪ
2NaCl+2H2O
2NaOH+H2��+Cl2��
| ||
2NaCl+2H2O
2NaOH+H2��+Cl2��
��
| ||
��3��������״����2.24L��Fͨ��150mL 1.0m1?L-1��K��Һ�У���ַ�Ӧ�����Һ�����ԣ��������ʼ������ʵ����ֱ�Ϊ
Na2SO3Ϊ0.05mol��NaHSO3Ϊ0.05mol
Na2SO3Ϊ0.05mol��NaHSO3Ϊ0.05mol
����4����F���Ԫ����ͬ��һ��-2���������M��M������Ԫ�ص�������Ϊ4��3����֪1mol A�����뺬1mol M����Һ��ǡ����ȫ��Ӧ����Ӧʱ���۲쵽��dz��ɫ����������ȡ��Ӧ����ϲ���Һ���������ữ���Ȼ�����Һ���а�ɫ������������A�����뺬M����Һ��Ӧ�����ӷ���ʽΪ
Cl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-
Cl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-
����������J��Ԫ��ԭ�Ӻ���ֻ��һ������֪JΪH2��
I����ɫ��ӦΪ��ɫ������I��NaԪ�أ�
�ɽ���B��A������ȼ�ղ����ػ�ɫ�̿�֪AΪCl2��BΪFe��Cu����DΪFeCl3��CuCl2��
��D+G+H2O��H+I+J�����I��NaԪ��֪GΪ�����ƣ���H2O+G��K+J��H2��������KΪNaOH��
D��ˮ��Һ���ػ�ɫ����DΪFeCl3����ˮ��Һ��Na�ķ�ӦΪ��
6Na+2FeCl3+6H2O�T2Fe��OH��3��+6NaCl+3H2����
FΪ��ɫ���д̼�����ζ���壬����ʹƷ����Һ��ɫ��ӦΪSO2����CΪH2SO4��EΪFe2��SO4��3��HΪFe��OH��3��LΪNaCl���Դ˽����⣮
I����ɫ��ӦΪ��ɫ������I��NaԪ�أ�
�ɽ���B��A������ȼ�ղ����ػ�ɫ�̿�֪AΪCl2��BΪFe��Cu����DΪFeCl3��CuCl2��
��D+G+H2O��H+I+J�����I��NaԪ��֪GΪ�����ƣ���H2O+G��K+J��H2��������KΪNaOH��
D��ˮ��Һ���ػ�ɫ����DΪFeCl3����ˮ��Һ��Na�ķ�ӦΪ��
6Na+2FeCl3+6H2O�T2Fe��OH��3��+6NaCl+3H2����
FΪ��ɫ���д̼�����ζ���壬����ʹƷ����Һ��ɫ��ӦΪSO2����CΪH2SO4��EΪFe2��SO4��3��HΪFe��OH��3��LΪNaCl���Դ˽����⣮
����⣺��J��Ԫ��ԭ�Ӻ���ֻ��һ������֪JΪH2��
I����ɫ��ӦΪ��ɫ������I��NaԪ�أ�
�ɽ���B��A������ȼ�ղ����ػ�ɫ�̿�֪AΪCl2��BΪFe��Cu����DΪFeCl3��CuCl2��
��D+G+H2O��H+I+J�����I��NaԪ��֪GΪ�����ƣ���H2O+G��K+J��H2��������KΪNaOH��
D��ˮ��Һ���ػ�ɫ����DΪFeCl3����ˮ��Һ��Na�ķ�ӦΪ��
6Na+2FeCl3+6H2O�T2Fe��OH��3��+6NaCl+3H2����
FΪ��ɫ���д̼�����ζ���壬����ʹƷ����Һ��ɫ��ӦΪSO2����CΪH2SO4��EΪFe2��SO4��3��HΪFe��OH��3��LΪNaCl��
��1��AΪCl��λ�ڵ�3���ڢ�A�壬KΪNaOH�������Ӽ����ۼ������Թ��ۼ�����
�ʴ�Ϊ����3���ڢ�A�壻���Ӽ����ۼ������Թ��ۼ�����
��2����D��ˮ��Һ��G��Ӧ�����ӷ���ʽΪCu2++2H2O+2Na�TCu��OH��2��+2Na++H2������д2Na+2H2O�T2Na++2OH-+H2����Cu2++2OH-�TCu��OH��2��Ҳ�ɣ���
�ʴ�Ϊ��Cu2++2H2O+2Na�TCu��OH��2��+2Na++H2����
�ڹ�ҵ��ͬʱ��ȡA���ʺ�K�ķ�Ӧ�Ļ�ѧ����ʽΪ2NaCl+2H2O
2NaOH+H2��+Cl2����
�ʴ�Ϊ��2NaCl+2H2O
2NaOH+H2��+Cl2����
��3��0.1molSO2��0.15molNaOH��Ӧ����������������xmol������������ymol����
��
���x=0.05mol��y=0.05mol��
�ʴ�Ϊ��Na2SO3Ϊ0.05 mol��NaHSO3Ϊ0.05 mol��
��4����F���Ԫ����ͬ��һ��-2���������M��M������Ԫ�ص�������Ϊ4��3����MΪS2O32-��F��M�����ӷ�ӦΪCl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-��
�ʴ�Ϊ��Cl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-��
I����ɫ��ӦΪ��ɫ������I��NaԪ�أ�
�ɽ���B��A������ȼ�ղ����ػ�ɫ�̿�֪AΪCl2��BΪFe��Cu����DΪFeCl3��CuCl2��
��D+G+H2O��H+I+J�����I��NaԪ��֪GΪ�����ƣ���H2O+G��K+J��H2��������KΪNaOH��
D��ˮ��Һ���ػ�ɫ����DΪFeCl3����ˮ��Һ��Na�ķ�ӦΪ��
6Na+2FeCl3+6H2O�T2Fe��OH��3��+6NaCl+3H2����
FΪ��ɫ���д̼�����ζ���壬����ʹƷ����Һ��ɫ��ӦΪSO2����CΪH2SO4��EΪFe2��SO4��3��HΪFe��OH��3��LΪNaCl��
��1��AΪCl��λ�ڵ�3���ڢ�A�壬KΪNaOH�������Ӽ����ۼ������Թ��ۼ�����
�ʴ�Ϊ����3���ڢ�A�壻���Ӽ����ۼ������Թ��ۼ�����
��2����D��ˮ��Һ��G��Ӧ�����ӷ���ʽΪCu2++2H2O+2Na�TCu��OH��2��+2Na++H2������д2Na+2H2O�T2Na++2OH-+H2����Cu2++2OH-�TCu��OH��2��Ҳ�ɣ���
�ʴ�Ϊ��Cu2++2H2O+2Na�TCu��OH��2��+2Na++H2����
�ڹ�ҵ��ͬʱ��ȡA���ʺ�K�ķ�Ӧ�Ļ�ѧ����ʽΪ2NaCl+2H2O
| ||
�ʴ�Ϊ��2NaCl+2H2O
| ||
��3��0.1molSO2��0.15molNaOH��Ӧ����������������xmol������������ymol����
|
���x=0.05mol��y=0.05mol��
�ʴ�Ϊ��Na2SO3Ϊ0.05 mol��NaHSO3Ϊ0.05 mol��
��4����F���Ԫ����ͬ��һ��-2���������M��M������Ԫ�ص�������Ϊ4��3����MΪS2O32-��F��M�����ӷ�ӦΪCl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-��
�ʴ�Ϊ��Cl2+S2O32-+H2O�T2Cl-+2H++S��+SO42-��
���������⿼��������ƶϣ���Ŀ�Ѷ��еȣ�������Ĺؼ�����ȷ�ƶ����ʵ����࣬�������ʵ����ʽ��ע���������ʵ���ɫ��ʵ�������ƶ�����Ϊ���Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
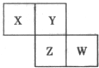 ��2012?��ɽ��ģ��X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ������λ����ͼ��ʾ����Yԭ�ӵ��������������ڲ��������3��������˵������ȷ���ǣ�������
��2012?��ɽ��ģ��X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ������λ����ͼ��ʾ����Yԭ�ӵ��������������ڲ��������3��������˵������ȷ���ǣ�������