摘要:1] NH4+.Al3+.Mg2+ Cu2+Fe2+HCO3- K+Cl-SO42- (3)①略 ②略 ③略 (4)NH4+︰Mg2+︰Al3+=0.01︰0.02︰0.01=1︰2︰1
网址:http://m.1010jiajiao.com/timu3_id_351165[举报]
写出下列反应的化学方程式:
(1)过氧化钠与二氧化碳:
(2)二氧化硫与氧气:
(3)铜与浓硫酸:
 (标出电子转移的方向和数目).
(标出电子转移的方向和数目).
查看习题详情和答案>>
(1)过氧化钠与二氧化碳:
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
.(2)二氧化硫与氧气:
2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
.
| ||
| △ |
(3)铜与浓硫酸:


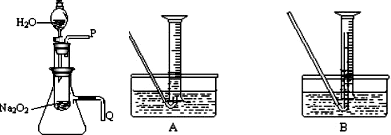 (2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一:有氧气生成;第二:
该反应是放热反应
该反应是放热反应
.Na2O2跟水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(2)某研究性学习小组拟用右图所示装置(气密性良好)
进行实验,以证明上述结论.
用以验证第一条结论的实验操作是:
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
;用以验证第二条结论的实验方法是:
将导管Q浸入水中,反应过程中导管口有气泡冒出
将导管Q浸入水中,反应过程中导管口有气泡冒出
.(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性.请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:
MnO2
MnO2
;现象:气泡迅速产生,能使带火星的木条复燃
气泡迅速产生,能使带火星的木条复燃
.(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论.
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)
B
B
(填序号),理由是防止气体冷却时发生倒吸现象
防止气体冷却时发生倒吸现象
.②若在标准状况下测量气体的体积,应选用的量筒的大小规格为
500mL
500mL
(选填“100mL”“200mL”“500mL”或“1000mL”).在呼吸面具和潜水艇中可以用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,用图中实验装置,进行实验来证明过氧化钠可作供氧剂.其中,A是实验室制取CO2的装置,D中装有过氧化钠固体.

(1)写出A装置中发生反应的离子方程式:
(2)填写表中空格:
(3)若无C装置,对实现该实验目的是否有影响
(4)试管F中收集满气体并从水中取出后,下一步实验操作为:
查看习题详情和答案>>

(1)写出A装置中发生反应的离子方程式:
CaCO3+2H+=Ca2++H2O+CO2↑
CaCO3+2H+=Ca2++H2O+CO2↑
;(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2中的HCl 除去CO2中的HCl |
| C | 浓硫酸 浓硫酸 |
除去CO2中的水蒸气 |
| E | NaOH溶液 NaOH溶液 |
除去O2中的CO2 除去O2中的CO2 |
否
否
(填“是”或“否”),原因2Na2O2+2H2O=4NaOH+O2
2Na2O2+2H2O=4NaOH+O2
;(4)试管F中收集满气体并从水中取出后,下一步实验操作为:
立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气
立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气
.写出下列反应化学方程式或离子方程式
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为
(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为
(3)氢氧化亚铁被氧气氧化的化学方程式
(4)“雷雨发庄稼”有哪些科学道理,试解释原因(用有关反应的化学方程式表示):
(5)实验室制氨气的化学方程式:
(6)铜与浓硝酸反应的离子方程式:
查看习题详情和答案>>
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
;(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
;(3)氢氧化亚铁被氧气氧化的化学方程式
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
;(4)“雷雨发庄稼”有哪些科学道理,试解释原因(用有关反应的化学方程式表示):
N2+O2
2NO、2NO+O2═2NO2 、3NO2+H2O═2HNO3+NO
| ||
N2+O2
2NO、2NO+O2═2NO2 、3NO2+H2O═2HNO3+NO
;
| ||
(5)实验室制氨气的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;
| ||
(6)铜与浓硝酸反应的离子方程式:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
.写出下列反应的离子方程式
(1)过氧化钠与水
(2)金属铝与稀硫酸溶液
(3)向Na2CO3与NaHCO3 混和溶液加入CaCl2溶液
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示有关生成H2的变化:
(A)
(B)
查看习题详情和答案>>
(1)过氧化钠与水
2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
;(2)金属铝与稀硫酸溶液
2Al+6H+=2Al3++3H2↑
2Al+6H+=2Al3++3H2↑
;(3)向Na2CO3与NaHCO3 混和溶液加入CaCl2溶液
Ca2++CO32-=CaCO3↓
Ca2++CO32-=CaCO3↓
;(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示有关生成H2的变化:
(A)
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
,(B)
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.