摘要:(三)碱金属的相似性.递变性 碱 r<r<r<r 金 金 熔 密 较慢 较缓慢 子 被空气O2氧化 与H2O反应 属 属 沸 度 很快 剧烈 性 r<r<r 3Li 性 键 点 递 渐 剧烈 r<r<r<r 剧烈 11Na 递 减 降 增 剧烈 增 剧烈 燃烧 19K 自燃 爆炸 伴随 r<r< r<r 37Rb 增 弱 低 55Cs 区分碱金属投入水中产生现象的异同: 现象: Li Na K Ru.Cs 共同点 浮.熔.游. 气. 红 沉 不同点: 不熔 熔 火球.轻微爆炸 立即燃烧 甚至爆炸 逐渐消失 很快消失
网址:http://m.1010jiajiao.com/timu3_id_350120[举报]
已知SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;镁和钠的化学性质也有一定的相似性.氧化铜和氧化铁是碱性氧化物,化学性质相似.三个研究性学习小组分别根据不同的微型课题进行研究,其方案如下:
I.第一个研究性学习小组用如图I所示的装置进行镁与二氧化硫反应的实验.
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:
A.10%的硫酸 B.95%的硫酸 C.浓盐酸D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体 G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中,产生具有臭鸡蛋气味的气体,写出在B管中发生的有关化学反应方程式:
(3)提出该装置的不足之处并写出改进方法:
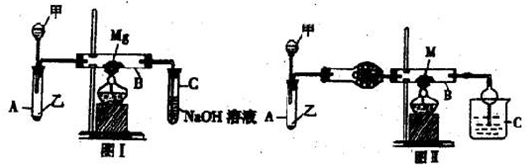
Ⅱ.第二个研究性学习小组利用I装置(图I)进行适当改进(图Ⅱ)来探究氨气的还原性.
(4)分别注明所用试剂:甲
Ⅲ. 第三个研究性学习小组认为第1I组实验装置(图II)中在A、C处添加加热装置就可以验证:乙醇在加热条件下能否被氧化铁氧化,且验证主要产物.
(5)C处的加热方法是
查看习题详情和答案>>
I.第一个研究性学习小组用如图I所示的装置进行镁与二氧化硫反应的实验.
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:
BE
BE
.A.10%的硫酸 B.95%的硫酸 C.浓盐酸D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体 G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中,产生具有臭鸡蛋气味的气体,写出在B管中发生的有关化学反应方程式:
2Mg+SO2
2MgO+S,Mg+S
MgS
| ||
| ||
2Mg+SO2
2MgO+S,Mg+S
MgS
| ||
| ||
(3)提出该装置的不足之处并写出改进方法:
在A、B之间加一个干燥管
在A、B之间加一个干燥管
.
Ⅱ.第二个研究性学习小组利用I装置(图I)进行适当改进(图Ⅱ)来探究氨气的还原性.
(4)分别注明所用试剂:甲
浓氨水
浓氨水
,乙生石灰或氢氧化钠
生石灰或氢氧化钠
,M为氧化铜,C为水
水
.确认反应己发生的实验现象黑色氧化铜粉末变红色粉末,试管内壁有水珠
黑色氧化铜粉末变红色粉末,试管内壁有水珠
.Ⅲ. 第三个研究性学习小组认为第1I组实验装置(图II)中在A、C处添加加热装置就可以验证:乙醇在加热条件下能否被氧化铁氧化,且验证主要产物.
(5)C处的加热方法是
水浴加热烧杯
水浴加热烧杯
.分别注明试剂:甲为乙醇,M为氧化铁,C为银氨溶液
银氨溶液
,B中发生反应的化学方程式是3CH3CH2OH+Fe2O3
2Fe+3CH3CHO+3H2O
| △ |
3CH3CH2OH+Fe2O3
2Fe+3CH3CHO+3H2O
.| △ |
如图是元素周期表的一部分
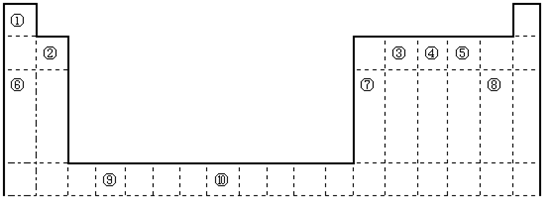
(1)上述元素中,属于s区元素的是 (填元素符号)
(2)元素④气态氢化物的中心原子有 对孤对电子,其VSEPR模型为 ;向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为 ;
(3)写出元素⑩的基态原子的价电子排布式 ,指出它在周期表中的位置 .焊接钢轨时,常利用⑩的某些氧化物与⑦的单质在高温下发生反应,试写出其中一种反应的化学方程式 ;
(4)①③⑤三种元素可以形成多种有机化合物分子,其中最简单原子数最少的一种是室内装潢时形成的主要气体污染物.试写出它的电子式 ;
(5)元素①可以与元素⑥形成化合物,试写出它的电子式 ;
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式 .
查看习题详情和答案>>

(1)上述元素中,属于s区元素的是
(2)元素④气态氢化物的中心原子有
(3)写出元素⑩的基态原子的价电子排布式
(4)①③⑤三种元素可以形成多种有机化合物分子,其中最简单原子数最少的一种是室内装潢时形成的主要气体污染物.试写出它的电子式
(5)元素①可以与元素⑥形成化合物,试写出它的电子式
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式
下表为长式周期表的一部分,其中的编号代表对应的元素.
试填空.
(1)写出上表中元素D形成单质的电子式为
 ;
;
(2)元素K基态原子的电子排布式
 ;元素D原子核外的电子占有的轨道数目为
;元素D原子核外的电子占有的轨道数目为
(3)元素M位于周期表的第
(4)G、H、I 这三种元素的第一电离能由大到小的顺序是
(5)元素A、D、J按照原子个数比4:1:1形成的化合物的化学式为
(6)A、C、D 形成的ACD分子中,含有
(7)E、F、G、H这四种元素原子形成的简单阴、阳离子,按半径由小到大排列
(8)某些不同族元素的性质也有一定的相似性,如上表中元素B与元素I的氢氧化物有相似的性质,写出元素B的氢氧化物与NaOH溶液反应后盐的化学式
(9)元素L在一定条件下形成的晶体的基本结构单元如图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:

查看习题详情和答案>>
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | ||||||||||||||
| K | M | L |
(1)写出上表中元素D形成单质的电子式为


(2)元素K基态原子的电子排布式
[Ar]3d54s1
[Ar]3d54s1
;H元素的离子结构示意图

5
5
个.(3)元素M位于周期表的第
ⅤⅢ
ⅤⅢ
族;当将M单质与酸性KMnO4溶液作用时,1个M原子失去3个电子,这些电子分别是在4s、3d
4s、3d
轨道上的;(4)G、H、I 这三种元素的第一电离能由大到小的顺序是
Mg>Al>Na
Mg>Al>Na
(填对应的元素符号);三种元素最高价氧化物对应水化物的碱性由强到弱排列NaOH>Mg(OH)2>Al(OH)3
NaOH>Mg(OH)2>Al(OH)3
(填对应的化学式).(5)元素A、D、J按照原子个数比4:1:1形成的化合物的化学式为
NH4Cl
NH4Cl
,其形成的晶体中含有的化学键类型为离子键和共价键、配位键
离子键和共价键、配位键
.(写出化学键最具体的类别)(6)A、C、D 形成的ACD分子中,含有
2
2
个σ键,2
2
个π键.(7)E、F、G、H这四种元素原子形成的简单阴、阳离子,按半径由小到大排列
Mg2+<Na+<F-<O2-
Mg2+<Na+<F-<O2-
(填对应的离子符号)(8)某些不同族元素的性质也有一定的相似性,如上表中元素B与元素I的氢氧化物有相似的性质,写出元素B的氢氧化物与NaOH溶液反应后盐的化学式
Na2BeO2
Na2BeO2
.(9)元素L在一定条件下形成的晶体的基本结构单元如图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:
2:3
2:3
.两种晶胞中实际含有原子个数之比为1:2
1:2
.
(2010?南开区一模)如表中的实线表示元素周期表的部分边界.①~⑩分别表示元素周期表中对应位置的元素.

(1)请在上表中用直尺画实线补全元素周期表边界.
(2)⑥、⑦、⑧、⑨的原子半径由大到小的顺序是
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被MnO2、FeCl3等催化分解,写出该化合物的电子式:
 .
.
(4)⑨、⑩各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(5)写出一种由①、⑤、⑥三种元素形成的常见无机化合物的名称
(6)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑨的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式:
查看习题详情和答案>>

(1)请在上表中用直尺画实线补全元素周期表边界.
(2)⑥、⑦、⑧、⑨的原子半径由大到小的顺序是
Mg>Al>O>F
Mg>Al>O>F
(填元素符号).(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被MnO2、FeCl3等催化分解,写出该化合物的电子式:


(4)⑨、⑩各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
Al(OH)3+3H+═Al3++3H2O
Al(OH)3+3H+═Al3++3H2O
.(5)写出一种由①、⑤、⑥三种元素形成的常见无机化合物的名称
硝酸
硝酸
;向水中加入少量该化合物,对水的电离起抑制
抑制
作用(填“抑制”、“促进”或“不影响”);原因是硝酸在水中电离产生H+,抑制水的电离
硝酸在水中电离产生H+,抑制水的电离
.(6)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑨的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式:
Be(OH)2+2NaOH=Na2BeO2+2H2O
Be(OH)2+2NaOH=Na2BeO2+2H2O
.又如表中与元素⑧的性质相似的不同族元素是Li
Li
(填元素符号)