网址:http://m.1010jiajiao.com/timu3_id_349898[举报]
为测定碳酸钙粉末的纯度(含杂质SiO2),某学校学生设计了如下几个实验方案:
方案一:①称取碳酸钙样品M g;②加入过量盐酸;③收集并测定生成的气体体积V mL。
方案二:①称取碳酸钙样品M g;②用c mol/L盐酸V mL(过量)溶解样品;③取溶解后的溶液用c′mol/L NaOH溶液滴定,恰用去V′ mL。
方案三:①称取碳酸钙样品M g;②高温1000 ℃煅烧直至质量不再改变,冷却后称量,质量为M′ g。
方案四:①称取碳酸钙样品M g;②加入足量c mol/L盐酸V mL使之完全溶解;③过滤并取滤液;④在滤液中加入过量的c′mol/L Na2CO3溶液V′mL;⑤将步骤④中的沉淀滤出,洗涤、干燥、称量为M′g。
依据以上实验方案回答以下问题:
(1)方案一中如果称量样品时,砝码底部有一处未被发现的残缺,那么测得的碳酸钙纯度会________(填“偏高”、“偏低”或“无影响”)。
(2)方案二中:列出本实验中所用到的仪器名称(除铁架台、烧杯、铁架台附件外)_________________________________________________________________________。
(3)方案三中的“冷却”应如何操作:
____________________________________________________________;
理由是_________________________________________________________。
(4)方案四中计算碳酸钙纯度的公式为______________;步骤⑤中要将沉淀进行洗涤,如果未经洗涤,则测定结果碳酸钙纯度将________(填“偏高”、“偏低”或“无影响”)。
(5)综上所述,请从实验条件的难易、操作引起实验误差的大小等方面进行综合判断,你认为四个方案中,最好的方案是________。其他方案的缺点分别是:
方案四:沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差。
方案________:_____________________________________________________。
方案________:____________________________________________________。
查看习题详情和答案>>
实验步骤如下:
步骤一:取16.6 g三硅酸镁样品,充分加热至不再分解,冷却、称量,得固体13. 0 g。
步骤二:另取16. 6 g三硅酸镁样品,向其中加入足量100 mL4 mol/L的盐酸,充分反应后,过滤,洗涤,灼烧得固体9.0g。该固体为空间网状结构且熔沸点很高。有关部门规定三硅酸镁样品中含水量不超过
12.2%为优良级。
(1)计算确定MgxSi3Oy·mH2O的化学式。
(2)该小组测定的三硅酸镁样品是否为优良级?
(3)写出该三硅酸镁样品与盐酸反应的化学方程式。
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.
[探究一]
实验方案:铝镁合金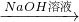 测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是______
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol?L-1NaOH溶液中,充分反应.NaOH溶液的体积V≥______
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将
______(填“偏高”或“偏低”).
[探究二]
实验方案:铝镁合金 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:
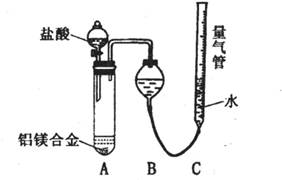
问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置.你的意见是:______(填“需要”或“不需要”).
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):①______②______
[探究三]
实验方案:称量x g铝镁合金粉末.放在如右图所示装置的惰性电热板上,通电使其充分灼烧.
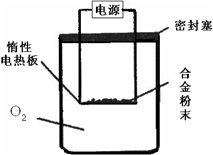 问题讨论:
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是______
(2)若用空气代替O2进行实验,对测定结果何影响?______(填“偏高”或“偏低”或“无影响”).
查看习题详情和答案>>
[探究一]
实验方案:铝镁合金
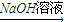 测定剩余固体质量
测定剩余固体质量实验中发生反应的化学方程式是______
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol?L-1NaOH溶液中,充分反应.NaOH溶液的体积V≥______
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将
______(填“偏高”或“偏低”).
[探究二]
实验方案:铝镁合金
 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置.你的意见是:______(填“需要”或“不需要”).
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):①______②______
[探究三]
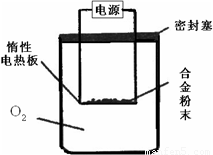
实验方案:称量x g铝镁合金粉末.放在如右图所示装置的惰性电热板上,通电使其充分灼烧.
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是______
(2)若用空气代替O2进行实验,对测定结果何影响?______(填“偏高”或“偏低”或“无影响”).

 查看习题详情和答案>>
查看习题详情和答案>>
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.
[探究一]
实验方案:铝镁合金![]() 测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是________
实验步骤:
(1)称取5.4 g铝镁合金粉末样品,投入V mL 2.0mol·L-1 NaOH溶液中,充分反应.NaOH溶液的体积V≥________.
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将________(填“偏高”或“偏低”)
[探究二]
实验方案:铝镁合金![]() 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:
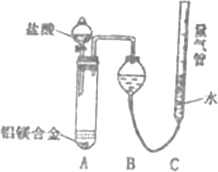
问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥,除酸雾的装置.你的意见是:________(填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
①________②________
[探究三]
实验方案:称量x g铝镁合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.
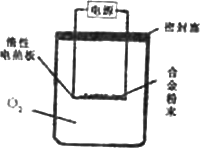
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是________
(2)若用空气代替O2进行实验,对测定结果何影响?________(填“偏高”或“偏低”或“无影响”)