网址:http://m.1010jiajiao.com/timu3_id_348927[举报]
如图所示的正立方体中有A~F六个点,其中点A处于立方体的中心,点B~F均处于立方体的顶点。
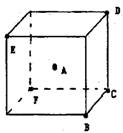
(1)请从A~F六个位置中选择合适的位置,放置相应的原子模型来表示CO2和CH4的分子空间构型。① 点放置碳原子, 点放置氧原子,可表示CO2的分子空间构型。② 点放置碳原子, 点放置氢原子,可表示CH4的分子空间构型。
(2)若如图所示的正立方体是某晶体的晶胞,A点是M原子,B、D、E、F均为N原子,C点无任何原子。则该晶体的化学式为:
查看习题详情和答案>>(1)E元素原子基态时的外围电子排布式为
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因是
(4)从晶胞结构图1中可以看出,D跟B形成的离子化合物的电子式为


| ||
| ρg?cm-3 |
| ||
| ρg?cm-3 |
(5)BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为
(6)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为

现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期,B元素原子的价层电子总数是内层电子总数的2倍;D元素原子的L电子层中只有两对成对电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子。请回答下列问题:
(1) E元素基态原子的核外价层电子排布式为_________。
(2)用元素符号表示B、C、D三种元素的第一电离能由低到高的排序_________。
(3) A元素与B、C元素可形成化合物B2A4、C2A4。
①B2A4的结构式为_________。
②下列有关C2A4的说法正确的是_________。
a.一个该分子中含有4个σ键
b.该分子可作为配位体形成配位键
c.该分子是非极性分子 d.1mol该分子最多可形成4mol氢键
e.该分子的稳定性与氢键无关
f.该分子中C的原子轨道是sp3杂化
(4)B单质的一种的晶体结构如图甲所示,E单质的一种的晶体结构如图乙所示。
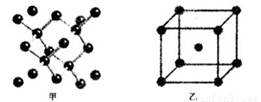
则图中的单质B的名称_________,图甲中B原子的配位数与图乙中E原子的配位数之_________。
E元素与D元素形成的ED晶体与NaCl晶体一样,欲比较ED与NaCl的晶格能大小,需考虑的数据是_______________________________________________________________________________。
(5)据最新资料显示,F单质的晶胞可能有多种,若其晶胞分别以六方紧密堆积和面心立方堆积存在时,其单质的密度之比为_________。
查看习题详情和答案>>
(1) E元素基态原子的核外价层电子排布式为_________。
(2)用元素符号表示B、C、D三种元素的第一电离能由低到高的排序_________。
(3) A元素与B、C元素可形成化合物B2A4、C2A4。
①B2A4的结构式为_________。
②下列有关C2A4的说法正确的是_________。
a.一个该分子中含有4个σ键
b.该分子可作为配位体形成配位键
c.该分子是非极性分子 d.1mol该分子最多可形成4mol氢键
e.该分子的稳定性与氢键无关
f.该分子中C的原子轨道是sp3杂化
(4)B单质的一种的晶体结构如图甲所示,E单质的一种的晶体结构如图乙所示。

则图中的单质B的名称_________,图甲中B原子的配位数与图乙中E原子的配位数之_________。
E元素与D元素形成的ED晶体与NaCl晶体一样,欲比较ED与NaCl的晶格能大小,需考虑的数据是_______________________________________________________________________________。
(5)据最新资料显示,F单质的晶胞可能有多种,若其晶胞分别以六方紧密堆积和面心立方堆积存在时,其单质的密度之比为_________。
已知:
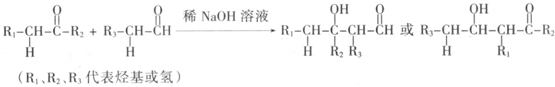
有机物A~H的转化关系如下图所示:

其中:①A不能使溴的四氯化碳溶液褪色,其核磁共振氢谱为单峰
②E、F互为同分异构体
请回答:
(1)C的化学名称是
(2)由D生成E或F的反应类型是
(3)下列关于G的说法正确的是
a.G可与FeCl3溶液发生显色反应
b.一定条件下,G可发生消去反应
c.1mol G与足量NaOH溶液反应,最多消耗2mol NaOH
d.在Cu催化、加热条件下,G可发生催化氧化反应
(4)由C生成D的化学方程式为
(5)由G生成H的化学方程式为
(6)同时满足下列条件的E的同分异构体有
a.属于酯类 b.含有六碳环结构 c.六碳环上只有一个取代基.