摘要: 硫铁矿高温下被空气氧化产生二氧化硫:4FeS2 + 11O2→8SO2 + 2Fe2O3 设空气中N2.O2的含量分别为0.800和0.200(体积分数.以下气体含量均用体积分数表示).试完成下列各题: (1)1.00molFeS2完全氧化.需要空气的体积为 L. (2)55L空气和足量FeS2完全反应后.气体体积变为 L. (3)用空气氧化FeS2产生的气体混合物中.O2的含量为0.0800.计算SO2的含量. (4)设FeS2氧化产生的气体混合物为100L.其中O2为a L.SO2为b L. ①写出a和b的关系式 ②在右图中画出a和b的关系曲线(FeS2氧化时.空气过量20%) 说明:为方便作图.纵坐标用13b表示.
网址:http://m.1010jiajiao.com/timu3_id_347897[举报]
硫铁矿高温下被空气氧化产生二氧化硫:4FeS2+11O2=8SO2+2Fe2O3。设空气中N2、O2的含量分别为?0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00 mol FeS2被完全氧化,需要空气的体积(标准状况)为________L。
(2)
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.080 0,计算SO2的含量。
(4)设氧化FeS2产生的气体混合物为

说明:为方便作图,纵坐标用13 b表示。
查看习题详情和答案>>
硫铁矿高温下被空气氧化产生二氧化硫:4FeS2+11O2====8SO2+2Fe2O3。设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00 mol FeS2被完全氧化,需要空气的体积(标准状况)为_________L。
(2)55 L空气和足量FeS2完全反应后,气体体积(同温同压)变为__________L。
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.0800,计算SO2的含量。
(4)设氧化FeS2产生的气体混合物为100 L,其中O2为a L,SO2为b L。①写出a和b的关系式。②在下图中画出a和b的关系曲线(氧化FeS2时,空气过量20%)。

说明:为方便作图,纵坐标用13b表示。
查看习题详情和答案>>二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义.
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
8SO2+2Fe2O3,该反应中被氧化的元素是______(填元素符号).当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为______L.
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)
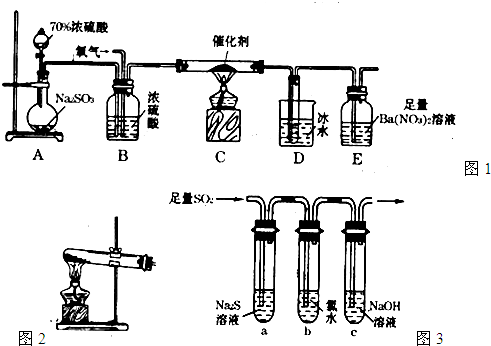
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______.
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式______.
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______.
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为______.
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是______(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______.
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示).
查看习题详情和答案>>
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
| ||
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______.
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式______.
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______.
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为______.
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是______(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______.
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示).
(2013?临沂一模)二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义.
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
8SO2+2Fe2O3,该反应中被氧化的元素是
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)
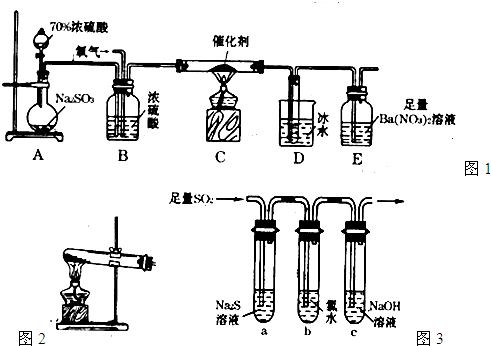
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
×100%
×100%(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=
查看习题详情和答案>>
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
| ||
Fe、S
Fe、S
(填元素符号).当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为11.2
11.2
L.(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是
打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加
打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加
.②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.
| ||
| △ |
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
使残留在装置中的二氧化硫和三氧化硫被充分吸收
使残留在装置中的二氧化硫和三氧化硫被充分吸收
.④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
| ||||
|
| ||||
|
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为
试管a中出现淡黄色浑浊
试管a中出现淡黄色浑浊
.②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
Ⅲ
Ⅲ
(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为SO2+Cl2+2H2O=4H++SO42-+2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
.③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=
2c(SO32-)+c(HSO3-)
2c(SO32-)+c(HSO3-)
(用含硫微粒浓度的代数式表示).盐酸、硫酸和硝酸是中学阶段常见的“三大酸”,请就“三大酸”的性质,回答下列问题:
(1)稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解.该反应的化学方程式为
(2)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO.其实验流程图如下:

①若要测定NO的体积,从图所示的装置中,你认为应选用
②选用如图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置
(3)工业制硫酸时,硫铁矿(FeS2)高温下空气氧化产生二氧化硫:4FeS2+11O2=8SO2+2Fe2O3,设空气中N2、O2的含量分别为0.800和0.200(体积分数),4.8t FeS2完全制成硫酸,需要空气的体积(标准状况)为
查看习题详情和答案>>
(1)稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解.该反应的化学方程式为
Cu+H2O2+2HCl═CuCl2+2H2O
Cu+H2O2+2HCl═CuCl2+2H2O
.(2)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO.其实验流程图如下:

①若要测定NO的体积,从图所示的装置中,你认为应选用
A
A
装置进行Cu与浓硝酸反应实验,选用的理由是因为A装置可以通N2将装置中的空气排尽,防止NO被空气中O2氧化
因为A装置可以通N2将装置中的空气排尽,防止NO被空气中O2氧化
.②选用如图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
123547
123547
(填各导管口编号).123547
123547
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置
升高
升高
(“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平.(3)工业制硫酸时,硫铁矿(FeS2)高温下空气氧化产生二氧化硫:4FeS2+11O2=8SO2+2Fe2O3,设空气中N2、O2的含量分别为0.800和0.200(体积分数),4.8t FeS2完全制成硫酸,需要空气的体积(标准状况)为
1.68×107
1.68×107
L.