题目内容
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义.
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
8SO2+2Fe2O3,该反应中被氧化的元素是______(填元素符号).当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为______L.
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)
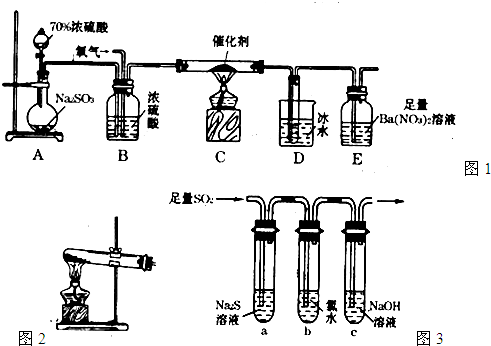
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______.
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式______.
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______.
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为______.
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是______(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______.
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示).
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2
| ||
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率.(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______.
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式______.
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______.
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简).
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为______.
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是______(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______.
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示).
(1)氧化还原反应4FeS2+11O2
8SO2+2Fe2O3中,化合价升高的Fe、S元素在反应中被氧化,该反应生成8mol的二氧化硫,转移电子的物质的量为44mol,所以当该反应转移2.75mol电子时,生成的二氧化硫的物质的量为0.5mol,在标准状况下的体积为11.2L,故答案为:Fe、S;11.2;
(2)①分液漏斗的使用方法:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加,故答案为:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加;
②氯用图2所示装置制取氧气,即加热固体的方法制氧气,可以让氯酸钾在二氧化锰催化下受热分解获得氧气,方程式为:2KClO3
2KCl+O2↑,
故答案为:2KClO3
2KCl+O2↑;
③为确保实验的准确度,要保证二氧化硫和三氧化硫的量的测定准确,当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,可以让装置中的二氧化硫和三氧化硫充分被后面的装置吸收,故答案为:使残留在装置中的二氧化硫和三氧化硫被充分吸收;
④装置D增加的质量为mg,及生成三氧化硫的质量是mg,物质的量是
,装置E中产生白色沉淀的质量为ng,则吸收的二氧化硫的物质的量是
,则二氧化硫的转化率=
×100%,故答案为:
×100%;
(3)①二氧化硫具有氧化性,可以和最低价的硫化钠发生氧化还原反应,生成淡黄色的沉淀S,故答案为:试管a中出现淡黄色浑浊;
②方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成,可能是氯水中的氯离子产生的作用,
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去,可以是氯水中含有的漂白性物质次氯酸起的作用;
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀,证明溶液汇总出现硫酸根离子,是二氧化硫在酸性环境下和氯水反应生成的,即SO2+Cl2+2H2O=4H++SO42-+2Cl-,故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;
③将二氧化硫通入到盛有氢氧化钠的试管c中,所得溶液中存在电荷守恒:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),溶液显示中性,所以c(H+)=c(OH-),此时:c(Na+)=2c(SO32-)+c(HSO3-),故答案为:2c(SO32-)+c(HSO3-).
| ||
(2)①分液漏斗的使用方法:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加,故答案为:打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,慢慢滴加;
②氯用图2所示装置制取氧气,即加热固体的方法制氧气,可以让氯酸钾在二氧化锰催化下受热分解获得氧气,方程式为:2KClO3
| ||
| △ |
故答案为:2KClO3
| ||
| △ |
③为确保实验的准确度,要保证二氧化硫和三氧化硫的量的测定准确,当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,可以让装置中的二氧化硫和三氧化硫充分被后面的装置吸收,故答案为:使残留在装置中的二氧化硫和三氧化硫被充分吸收;
④装置D增加的质量为mg,及生成三氧化硫的质量是mg,物质的量是
| mg |
| 80g/mol |
| ng |
| 233g/mol |
| ||||
|
| ||||
|
(3)①二氧化硫具有氧化性,可以和最低价的硫化钠发生氧化还原反应,生成淡黄色的沉淀S,故答案为:试管a中出现淡黄色浑浊;
②方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成,可能是氯水中的氯离子产生的作用,
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去,可以是氯水中含有的漂白性物质次氯酸起的作用;
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀,证明溶液汇总出现硫酸根离子,是二氧化硫在酸性环境下和氯水反应生成的,即SO2+Cl2+2H2O=4H++SO42-+2Cl-,故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;
③将二氧化硫通入到盛有氢氧化钠的试管c中,所得溶液中存在电荷守恒:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),溶液显示中性,所以c(H+)=c(OH-),此时:c(Na+)=2c(SO32-)+c(HSO3-),故答案为:2c(SO32-)+c(HSO3-).

练习册系列答案
相关题目
 ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。


 8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。


 ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。
 ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。

