网址:http://m.1010jiajiao.com/timu3_id_347727[举报]
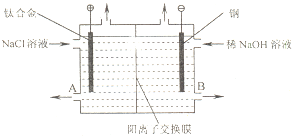 电解食盐水使用的离子交换膜电解槽装置如图所示.经过净化精制的饱和食盐水不断送入阳极室,向阴极室不断加入稀NaOH溶液.阳离子交换膜具有很好的选择性,它只允许阳离子通过.
电解食盐水使用的离子交换膜电解槽装置如图所示.经过净化精制的饱和食盐水不断送入阳极室,向阴极室不断加入稀NaOH溶液.阳离子交换膜具有很好的选择性,它只允许阳离子通过.(1)不能用普通钢代替钛合金做阳极的原因是(用电极反应式表示)
(2)在实际生产中,阳极得到气体的体积总是小于阴极所得气体体积,导致该现象的可能原因是
(3)一氯碱厂每天消耗234tNaCl.
①这些NaCl能生产质量分数为32%的NaOH溶液多少吨?
②若将该厂每天产生的H2、Cl2在一定条件下反应生成的HCl溶于水,可制得物质的量浓度为11.50mol/L的盐酸的体积为(假定生产中H2、Cl2的利用率均为92%.计算结果均保留3位有效数字)
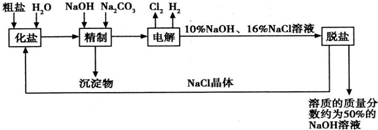
请回答下列问题:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为
(2)粗盐中含Ca2+、Mg2+等杂质.精制过程中发生反应的离子方程式为
(3)为有效除去Ca2+、Mg2+和S
| O | 2- 4 |
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3,
C.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(5)采用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜法电解食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学反应方程式为
| ||
| ||
 工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:(1)A极为电解槽的
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及Ca2+、Mg2+、Fe3+、SO42-等杂质,因此必须精制.精制时所用试剂为①NaOH ②Na2CO3 ③BaCl2④盐酸,这四种试剂的添加顺序为
(4)若将标准状况下6.72升阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是0.5×6.02×1023,产物中得到了两种含氯化合物,写出该反应的离子方程式:
| ||
| ||
(14分)工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的液体是 。

(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s)![]() 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气 ![]() (标准状况)。
(标准状况)。
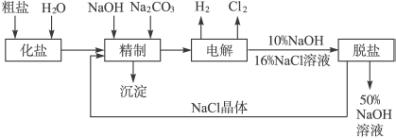
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的方程式为___________________。与电源负极相连的电极附近溶液Ph_________(填“不变”“升高”或“降低”)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程中发生反应的离子方程式为______________。
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该试剂可以是_____________。
,该试剂可以是_____________。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为___________(选a、b、c)。
,加入试剂的合理顺序为___________(选a、b、c)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过___________、冷却、_________(填写操作名称)除去NaCl。
(6)在用阳离子交换膜法电解食盐水时,电解槽分隔为阳极区和阴极区,可防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分反应,产物最终仅有NaClO和H2,相应的化学反应方程式为___________________________、_______________________。
查看习题详情和答案>>