网址:http://m.1010jiajiao.com/timu3_id_345675[举报]
(1)工业制硫酸的过程中,SO2被氧气氧化的化学方程式为
(2)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫.
已知:25℃时,H2SO3?HSO3-+H+K=1.5×10-2
H2CO3?HCO3-+H+K=4.4×10-7
①下列试剂中适合用作该法吸收剂的是
a.石灰乳 b.Na2SO3溶液 c.Na2CO3溶液
②“钠碱法”用NaOH溶液作吸收剂,向100mL 0.2mol?L-1的NaOH溶液中通入标准状况下0.448L SO2气体,反应后测得溶液pH<7,则溶液中下列各离子浓度关系正确的是
a.c(HSO3-)>c(SO32-)>c(H2SO3)
b.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
c.c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-)
(3)某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品.具体流程如下:
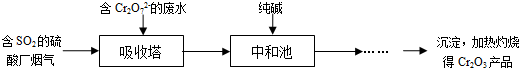
①吸收塔中反应后的铬元素以Cr3+形式存在,则其中发生反应的离子方程式为
②中和池中的反应除生成Cr(OH)3沉淀外,还会产生某种气体,该气体的化学式为
硫酸工厂的烟气中含有SO2,有多种方法可实现烟气脱硫。
(1)工业制硫酸的过程中,SO2被氧气氧化的化学方程式为 。
(2)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。
已知:25℃时,H2SO3
 HSO3 -+H+
K=1.5×10-2
HSO3 -+H+
K=1.5×10-2
H2CO3 HCO3 -+H+ K=4.4×10-7
HCO3 -+H+ K=4.4×10-7
下列试剂中适合用作该法吸收剂的是 (填字母序号)。
a.石灰乳 b. Na2SO3溶液 c. Na2CO3溶液
②“钠碱法”用NaOH溶液作吸收剂,向100 mL 0.2 mol·L-1 的NaOH溶液中通入标准状况下0.448 L SO2气体,反应后测得溶液pH<7,则溶液中下列各离子浓度关系正确的是 (填字母序号)。
a.c(HSO3-)> c(SO32-)> c(H2SO3)
b.c(Na+)>c(HSO3-)> c(H+)> c(SO32-)
c.c(Na+)+c(H+)= c(HSO3-)+c(SO32-)+c(OH-)
(3)某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品。具体流程如下:

①吸收塔中反应后的铬元素以Cr3+形式存在,则其中发生反应的离子方程式为 。
②中和池中的反应除生成Cr(OH)3沉淀外,还会产生某种气体,该气体的化学式为 。
查看习题详情和答案>>
Na+CO2![]() C(金刚石)+C(石墨)+Na2CO3,该法比1955年人工首次制得钻石的方法容易得多。原方法的化学原理是:C(石墨)
C(金刚石)+C(石墨)+Na2CO3,该法比1955年人工首次制得钻石的方法容易得多。原方法的化学原理是:C(石墨)![]() C(金刚石)。以下有关的表述中正确的是( )
C(金刚石)。以下有关的表述中正确的是( )
A.两方法利用的都是氧化还原反应
B.新法利用的是化学变化,旧法利用的是物理变化
C.两方法变化中都存在旧化学键的断裂与新化学键的形成
D.两方法变化中,金刚石都是还原产物,新法的Na2CO3是氧化产物
查看习题详情和答案>>(08芜湖模拟)中科大陈乾旺教授等人发现了人工合成金刚石的新方法,其化学原理为:
①Na+CO2 ![]() C(金刚石)+C(石墨)+Na2CO3(未配平)。
C(金刚石)+C(石墨)+Na2CO3(未配平)。
该法比1955年人工首次制得金刚石的方法容易得多,其化学原理是:
以下有关表述中正确的是()
A.反应①和②都存在旧化学键的断裂与新化学键的形成
B.新法利用的是化学变化,旧法利用的是物理变化
C.在反应①中每生成12g金刚石需要消耗23g金属钠
D.反应①和②中,金刚石都是还原产物,Na2CO3是氧化产物
查看习题详情和答案>>|
中科大陈乾旺教授等人发现了人工合成金刚石的新方法,其化学原理为: ①Na+CO2 该法比1955年人工首次制得金刚石的方法容易得多,其化学原理是:
以下有关表述中正确的是 | |
| [ ] | |
A. |
反应①和②都存在旧化学键的断裂与新化学键的形成 |
B. |
新法利用的是化学变化,旧法利用的是物理变化 |
C. |
在反应①中每生成12g金刚石需要消耗23g金属钠 |
D. |
反应①和②中,金刚石都是还原产物,Na2CO3是氧化产物 |