摘要: 在Na2SO4与K2SO4的混和溶液中.当[Na]= 0.2摩/升. SO = x 摩/升. K = y 摩/升.则x 和y 的关系是 ① x = 0.1+0.5y ② x = 0.5y ③ y = 2x-0.1 ④ y = 2 ①.④ ③.④
网址:http://m.1010jiajiao.com/timu3_id_34484[举报]
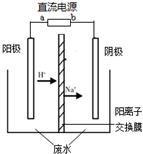 (2012?海淀区二模)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、电解阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO+H2O═CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.
(2012?海淀区二模)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、电解阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO+H2O═CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.(1)若以甲烷燃料电池为直流电源,则燃料电池中b极应通入
CH4
CH4
(填化学式)气体.(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体.电极反应如下:
阳极:①4OH--4e-═O2↑+2H2O
②
CH3CHO-2e-+H2O═CH3COOH+2H+
CH3CHO-2e-+H2O═CH3COOH+2H+
阴极:①
4H++4e-═2H2↑或4H2O+4e-═2H2↑+4OH-
4H++4e-═2H2↑或4H2O+4e-═2H2↑+4OH-
②CH3CHO+2e-+2H2O═CH3CH2OH+2OH-
(3)电解过程中,阴极区Na2SO4的物质的量
不变
不变
(填“增大”、“减小”或“不变”).(4)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同.下列关于阳极区溶液中各微粒浓度关系的说法正确的是
abd
abd
(填字母序号).a.c(Na+)不一定是c(SO42-)的2倍
b.c(Na+)=2c(CH3COOH)+2c(CH3COO-)
c.c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
d.c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(5)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃.从电解后阴极区的溶液中分离出乙醇粗品的方法是
蒸馏
蒸馏
.(6)在实际工艺处理中,阴极区乙醛的去除率可达60%.若在两极区分别注入1m3乙醛的含量为3000mg/L的废水,可得到乙醇
1.9
1.9
kg(计算结果保留小数点后1位).(2013?浙江模拟)某兴趣小组探究以芒硝(Na2SO4?10H2O)和CaO为原料制备Na2CO3.
(1)将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3.三元体系中反应的离子方程式为:
SO42-+Ca(OH)2+2H2O?CaSO4?2H2O+2OH-,△H=-15.6kJ?mol-1
该反应的平衡常数表达式K=
.
该反应在常温下不能自发进行,则可判断△S
(2)往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3[即c(OH-)为0.02mol?L-1],可使反应在常温下容易进行.反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3.
①在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是
②用平衡移动原理解释添加酸性物质的理由
以HA表示所添加的酸性物质,则总反应的离子方程式可写为
③添加的酸性物质须满足的条件(写出两点)是
④已知:某温度下,Ksp[Ca(OH)2]=5.2×10-6,Ksp(CaCaSO4)=1.3×10-4,设
的初始浓度为b mol?L-1,转化率为α,写出α与b的关系式
查看习题详情和答案>>
(1)将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3.三元体系中反应的离子方程式为:
SO42-+Ca(OH)2+2H2O?CaSO4?2H2O+2OH-,△H=-15.6kJ?mol-1
该反应的平衡常数表达式K=
| c2(OH-) |
| c(SO42-) |
| c2(OH-) |
| c(SO42-) |
该反应在常温下不能自发进行,则可判断△S
<
<
0 (填“>”或“<”).(2)往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3[即c(OH-)为0.02mol?L-1],可使反应在常温下容易进行.反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3.
①在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是
碱性条件下CO2与Ca2+生成难溶物CaCO3
碱性条件下CO2与Ca2+生成难溶物CaCO3
;②用平衡移动原理解释添加酸性物质的理由
酸性物质与OH-反应,使平衡向生成CaSO4?2H2O的方向进行
酸性物质与OH-反应,使平衡向生成CaSO4?2H2O的方向进行
;以HA表示所添加的酸性物质,则总反应的离子方程式可写为
SO42-+Ca(OH)2+2HA?CaSO4?2H2O↓+2A-
SO42-+Ca(OH)2+2HA?CaSO4?2H2O↓+2A-
.③添加的酸性物质须满足的条件(写出两点)是
不与Ca2+生成难溶物
不与Ca2+生成难溶物
、酸性比碳酸弱
酸性比碳酸弱
.④已知:某温度下,Ksp[Ca(OH)2]=5.2×10-6,Ksp(CaCaSO4)=1.3×10-4,设
| SO | 2- 4 |
α=
| b-0.01 |
| b |
α=
.| b-0.01 |
| b |
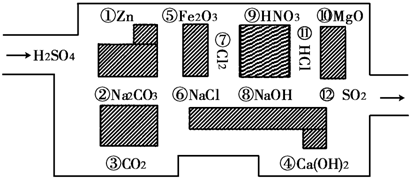
“探险队员”--稀硫酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多与稀硫酸反应的物质,稀硫酸必须避开它们,否则就无法通过.
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)
(2)在不能与稀硫酸反应的物质中,属于电解质的是
(3)稀硫酸遇到②Na2CO3时,若不能反应说明理由,若能反应写出反应的化学方程式
查看习题详情和答案>>
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)
③→⑥→⑦→⑨→?→?
③→⑥→⑦→⑨→?→?
.(2)在不能与稀硫酸反应的物质中,属于电解质的是
⑥⑨?
⑥⑨?
(填写物质前的序号);在能与稀硫酸反应的化学反应中,属于氧化还原反应的是Zn+2H+═Zn2++H2↑
Zn+2H+═Zn2++H2↑
(写出反应的离子方程式).(3)稀硫酸遇到②Na2CO3时,若不能反应说明理由,若能反应写出反应的化学方程式
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
.
在室温下,向Cu(IO3)2饱和溶液中加入足量的经稀硫酸酸化的KI溶液,产生CuI沉淀,溶液由蓝色变为棕黄色,反应前加入淀粉溶液不变蓝,反应后加入淀粉溶液变为蓝色.
(1)该反应中氧化剂是
(2)该反应的还原产物是
(3)1mol氧化剂在反应中得到电子的物质的量为
(4)某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4.请将NaBiO3之外的反应物与生成物分别填入以下空格内,配平化学计量数,并在氧化剂与还原剂之间标出电子转移的方向和数目.

查看习题详情和答案>>
(1)该反应中氧化剂是
Cu(IO3)2
Cu(IO3)2
;(2)该反应的还原产物是
CuII2
CuII2
;(3)1mol氧化剂在反应中得到电子的物质的量为
11mol
11mol
;(4)某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4.请将NaBiO3之外的反应物与生成物分别填入以下空格内,配平化学计量数,并在氧化剂与还原剂之间标出电子转移的方向和数目.

 (2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:
(2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2.
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数.
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100mL滴有淀粉的蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体积为20.00mL.求该黄铜矿的纯度.
(2)将FeS和Fe2O3的混和物56.6g,用足量稀H2SO4溶解后可得3.2g硫,求原混和物中FeS的质量.
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2.已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收.利用下图装置加热无水硫酸铜粉末直至完全分解.若无水硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示.
| 装置 | A (试管+粉末) |
B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4+4C
| 高温 |
| 高温 |
①若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量.
②硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量.