摘要:A(NH3的存在将促进SO32-的生成.而出现BaSO3,Cl2 .NO2的存在将使SO2氧化生成SO42-.而生成BaSO4) 13.AB 14.CD 15.BA 16.A 17.D (强碱的PH=13.强酸的PH=2.因为PH之和为15.故强碱和强酸的体积比按1:10混合时.混合液为中性.但题设条件为碱性.因此.强酸的体积应减少.故选D选项正确) 18.AB(由已知数据可知A正确,由S元素守恒和“等体积 混合可知.D正确) 19(1)3分.用镊子夹取白磷.在盛有水的水槽中切割 (2) BC(4分:只选一个得2分.选两个且都正确得4分.多选不得分)
网址:http://m.1010jiajiao.com/timu3_id_341930[举报]
氮化铝(AIN)是一种新型无机材料,广泛应用于集成电路生产领域.某化学研究小组利用 制取氮化铝,设计如图1所示的实验装置.
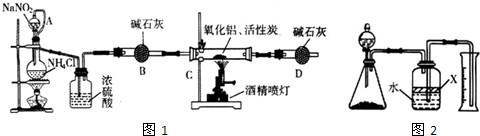
试回答:
(1)实验中用饱和NaNO2与 NH4C溶液制取氧气的化学方程式为 .
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是 (填写序号).
a.防止NaNO2 饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2 饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是 .
(4)化学研究小组的装置存在严重问题,请说明改进的办法 .
(5)反应结束后,某同学用图2所示装置进行实验来测定氮化铝样 品的质量分数(实验中导管体积忽略不计).已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气.
①广口瓶中的试剂X最好选用 (填写序号).a.汽油 b.酒精 c.植物油 d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将 (填“偏大”、“偏小”、“不变”).
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为 .
查看习题详情和答案>>

试回答:
(1)实验中用饱和NaNO2与 NH4C溶液制取氧气的化学方程式为
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是
a.防止NaNO2 饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2 饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是
(4)化学研究小组的装置存在严重问题,请说明改进的办法
(5)反应结束后,某同学用图2所示装置进行实验来测定氮化铝样 品的质量分数(实验中导管体积忽略不计).已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气.
①广口瓶中的试剂X最好选用
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为
(2011?江山市模拟)(背景材料)氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.氮化铝还是电绝缘体,介电性能良好,用作电器元件也很有希望.超细氮化铝粉末被广泛应用于大规模集成电路生产领域.其制取原理为:
Al2O3+3C+N2
2AlN+3CO
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为
②该样品中的AlN的质量分数为
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g?L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
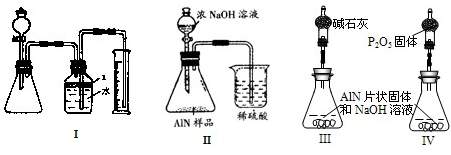
(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为
(2)本试验中检查装置气密性的方法是
(3)广口瓶中的试剂X可最好选用
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
%
%(AlN的式量为41).
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是
查看习题详情和答案>>
Al2O3+3C+N2
| 高温 |
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在
氧化铝
氧化铝
.问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为
AlN+NaOH+H2O=NaAlO2+NH3↑
AlN+NaOH+H2O=NaAlO2+NH3↑
.②该样品中的AlN的质量分数为
61.5%
61.5%
.(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g?L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳
1.92
1.92
g.问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)

(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为
③①②④
③①②④
.(2)本试验中检查装置气密性的方法是
关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落
关闭分液漏斗活塞,微热锥形瓶,广口瓶中右侧导管水柱上升,恒温时水柱并不回落
.(3)广口瓶中的试剂X可最好选用
C
C
(填选项的标号).A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
不变
不变
(填偏大、偏小或不变).(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
| 4100a |
| 22.4w |
| 4100a |
| 22.4w |
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
碳
碳
,为了测定是否含有其它杂质,则还需要哪些简单数据碳的质量
碳的质量
.问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
不可行
不可行
(填入“可行”、“不可行”),原因是II中NH3极易被吸收,发生倒吸现象,同时氨气中含有水蒸气,影响氨气质量的测定
II中NH3极易被吸收,发生倒吸现象,同时氨气中含有水蒸气,影响氨气质量的测定
.最简单的改进方法为在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气
在装置之间添加盛有碱石灰的干燥管,烧杯导管的末端接一倒扣的漏斗来吸收氨气
.问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是
反应产生的氨气不可能被完全吸收
反应产生的氨气不可能被完全吸收
.若忽略此原因的话,只要用图9中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为Ⅲ
Ⅲ
(填代号).你认为戊同学的装置是否还有缺陷?有
有
.若有,所测结果将偏高或偏低偏低
偏低
,应作如何改进?应再接一个与IV装置中完全相同的干燥管(或再接一个装有碱石灰的干燥管也行)
应再接一个与IV装置中完全相同的干燥管(或再接一个装有碱石灰的干燥管也行)
.(若无缺陷后两此格可不填).氮化铝(AIN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计下图实验装置。
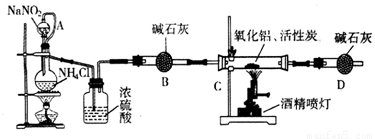
试回答:
(1)实验中用饱和NaNO2与 NH4C溶液制取氮气的化学方程式为 。
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是 (填写序号)。
a.防止NaNO2 饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2 饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是 。
(4)化学研究小组的装置存在严重问题,请说明改进的办法 。
(5)反应结束后,某同学用下图装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气
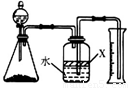 。
。
①广口瓶中的试剂X最好选用 (填写序号)。
a.汽油 b.酒精 c.植物油 d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将 (填“偏大”、“偏小”、“不变”)。
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为 。
查看习题详情和答案>>
氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.氮化铝还是电绝缘体,介电性能良好,用作电器元件也很有希望.超细氮化铝粉末被广泛应用于大规模集成电路生产领域.其制取原理为:
Al2O3+3C+N2 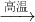 2AlN+3CO
2AlN+3CO
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在______.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为______.
②该样品中的AlN的质量分数为______.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g?L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳______g.
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)

(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为______.
(2)本试验中检查装置气密性的方法是______.
(3)广口瓶中的试剂X可最好选用______(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将______(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为______(AlN的式量为41).
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是______,为了测定是否含有其它杂质,则还需要哪些简单数据______.
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?______(填入“可行”、“不可行”),原因是______.最简单的改进方法为______.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是______.若忽略此原因的话,只要用图9中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为______(填代号).你认为戊同学的装置是否还有缺陷?______.若有,所测结果将偏高或偏低______,应作如何改进?______.(若无缺陷后两此格可不填).
查看习题详情和答案>>
(背景材料)氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.氮化铝还是电绝缘体,介电性能良好,用作电器元件也很有希望.超细氮化铝粉末被广泛应用于大规模集成电路生产领域.其制取原理为:
Al2O3+3C+N2
2AlN+3CO
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在______.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为______.
②该样品中的AlN的质量分数为______.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g?L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳______g.
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
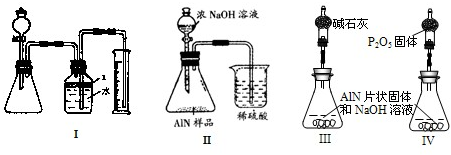
(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为______.
(2)本试验中检查装置气密性的方法是______.
(3)广口瓶中的试剂X可最好选用______(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将______(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为______(AlN的式量为41).
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是______,为了测定是否含有其它杂质,则还需要哪些简单数据______.
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?______(填入“可行”、“不可行”),原因是______.最简单的改进方法为______.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是______.若忽略此原因的话,只要用图9中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为______(填代号).你认为戊同学的装置是否还有缺陷?______.若有,所测结果将偏高或偏低______,应作如何改进?______.(若无缺陷后两此格可不填).
查看习题详情和答案>>
Al2O3+3C+N2
| 高温 |
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在______.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为______.
②该样品中的AlN的质量分数为______.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g?L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳______g.
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)

(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为______.
(2)本试验中检查装置气密性的方法是______.
(3)广口瓶中的试剂X可最好选用______(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将______(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为______(AlN的式量为41).
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是______,为了测定是否含有其它杂质,则还需要哪些简单数据______.
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?______(填入“可行”、“不可行”),原因是______.最简单的改进方法为______.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是______.若忽略此原因的话,只要用图9中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为______(填代号).你认为戊同学的装置是否还有缺陷?______.若有,所测结果将偏高或偏低______,应作如何改进?______.(若无缺陷后两此格可不填).