网址:http://m.1010jiajiao.com/timu3_id_33807[举报]
现有aA、bB、cC、dD、eE、fF六种短周期元素,原子序数依次增大,A、B、C、D都是生命不可缺少的重要元素。已知它们原子序数存在如下关系:a+b=c, a+c=d, b+c=f;元素A、B、C和D都能形成原子个数比为1:1和1:2的化合物;元素E的原子是短周期主族元素中原子半径最大的原子。其中由A、B、D三元素组成的化合物甲,其化学式灾BA4D;由D、E两元素形成原子个数比为1:1化合物乙;C的气态氢化物和最高价氧化物的水化物分别为丙和丁。请根据要求回答下列问题:
(1)经测定,A2D2的水溶液呈弱酸性。请写出第一步的电离方程式 。
(2)用甲和单质D2可设计成燃料电池,若电解质溶液为浓KOH溶液,则正极的电极反应式为 。
(3)3.9g乙与足量的水反应,电子转移的物质的量是 。
(4)单质F与E的最高价氧化物的水化物的溶液反应的离子方程式是 。
(5)常温下向25mL 0.1mol?L―1丙溶液中逐滴滴加0.1mol?L―1丁溶液,滴加过程中混合溶液pH的变化曲线如下图所示:

①图中m点由水电离也的OH―的物质的量浓度为 ;
②p点时,丙溶液和丁溶液恰好完全反应,则p点溶液中各备种离子浓度由大到小的顺序为 。
查看习题详情和答案>>
(1)溶液A中溶质的化学式________。
(2)他将样品放入托盘天平的右盘中,样品质量记录游码为
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是________。
(4)怎样证明滴加溶液A已经过量,简述操作方法________________。
(5)若物质C的质量为
植物生长需要营养,实验室现有一包由氯化铵和硫酸铵混合而成的白色粉末,课外小组的同学按下图设计进行实验,测定这种混合物中各组分的含量,以便给植物施用。
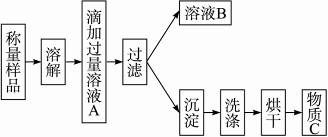
(1)溶液A中溶质的化学式________。
(2)他将样品放入托盘天平的右盘中,样品质量记录游码为0.4 g,左边的托盘里的砝码为16 g,则样品质量是________g。
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是________。
(4)怎样证明滴加溶液A已经过量,简述操作方法________________。
(5)若物质C的质量为23.3 g,那么原混合物中氯化铵的质量分数为________。
查看习题详情和答案>>(20分)A物质是实验室一种无色有毒的挥发性液体,由X、Y两种短周期元素组成。A在空气中极易着火生成B气体和C气体;A不溶于水,但加热到423K可以和水反应,生成B气体和D气体,D只含两种元素,其中一种是Y。在交流放电的情况下,分解生成E气体、F固体两种物质,E物质和B化学式量几乎相等,含Y元素约72.7%;F是环状单质分子,具有冠状结构,易溶于A,F的式量约是C的4倍。E可在液氮条件下与HBr于77K生成含双键结构的物质G,冷却至室温可得G的环状三聚体H。
6-1 写出A、B、C、D、E、F、G、H的结构简式。
6-2 用X射线衍射法测得F的晶体为正交晶系,晶胞参数a=1048pm,b=1292pm,c=2455pm。已知该物质的密度为2.07g?cm-3。计算每个晶胞中F分子的数目。
6-3 自发现富勒烯以来,其神奇的结构和性能引起了人们对碳原子团簇广泛和深入的研究。除了碳原子团簇之外,其它元素的原子团簇是否也具有类似碳原子团簇的奇异的特性,这是个十分有趣的研究课题。F物质有很多同分异构体,在实验手段受到各种条件的限制时,理论研究是一种重要的补充。厦门大学化学系对F物质的原子团簇进行了理论计算,发现除了冠状结构外还有多种结构。其中一种X具有2次对称轴,以及两个包含对称轴的对称面,一配位和三配位原子数目相等;另外一种Y是一种椅式结构原子团簇增加2个原子形成,也具有二次对称轴,对称面和对称轴垂直。请画出这两种结构的原子团簇。
6-4 五氟化砷AsF5(2.93g)和上述物质F(0.37g)用四氮化四硫S4N4(0.53g)在液态SO2溶剂中发生完全的反应,溶剂和挥发性产物被泵抽出后得黄色固体残留物L(3.08g),分析J知其含有:As 28.04%,F 42.70%,N 5.25%,经分析L是离子化合物,阴离子为正八面体结构,阳离子为两种元素组成,结构是直线形。固体L(0.48g)溶于液态二氧化硫,和叠氮化铯Cs+N3-(0.31g)完全反应,收集应释放出得氮气于66.5kPa、298K为67.1cm3。反应混合物过滤得难溶蓝黑色纤维状固体J(0.16g)。分析J知其含有2种元素,其中含N 30.3%。红外光谱、X射线粉末衍射结果表明抽出SO2后残留物是六氟砷(V)酸铯。
(1)L的实验式是什么?
(2)提出L的结构式;
(3)写出配平的生成L的方程式;
(4)1mol L发生转化时生成氮气的物质的量;
(5)J的化学式;
(6)写出n mol L生成J的普遍离子方程式。
查看习题详情和答案>>A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答
26.(A)实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从下图中选择制取气体的合适装置:

氮气 、氢气
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 、 
(3)氨合成器出来经冷却的气体连续通人乙装置的水中吸收氨, (“会”或“不会”)发生倒吸,原因是: 。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是: ,锥形瓶中还可观察到的现象是: 。
(5)写出乙装置中氨氧化的化学方程式:
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
(B)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:

(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上,不能直接放在桌面上。
实验所用仪器:a 蒸发皿 b 石棉网 c 泥三角 d 表面皿 e 坩埚钳 f 试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是
a 灼烧过程中部分氧化铜被还原 b 灼烧不充分铜未被完全氧化
c 氧化铜在加热过程中分解生成铜 d 该条件下铜无法被氧气氧化
(3)通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥
(4)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行 次
(6)若测定结果x值偏高,可能的原因是
a 加热温度过高 b 胆矾晶体的颗粒较大
c 加热后放在空气中冷却 d 胆矾晶体部分风化
查看习题详情和答案>>