题目内容
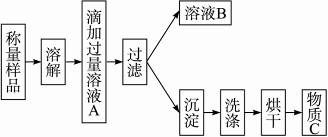
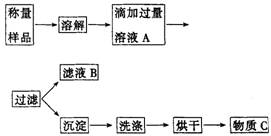
植物生长需要营养,实验室现有一包由氯化铵和硫酸铵混合而成的白色粉末,课外小组的同学按下图设计进行实验,测定这种混合物中各组分的含量,以便给植物施用。
(1)溶液A中溶质的化学式________。
(2)他将样品放入托盘天平的右盘中,样品质量记录游码为
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是________。
(4)怎样证明滴加溶液A已经过量,简述操作方法________________。
(5)若物质C的质量为
(1)BaCl2或Ba(NO3)2
(2)15.6
(3)玻璃棒
(4)取上层清液,逐滴加入稀H2SO4溶液,若观察到有沉淀生成,说明滴加的BaCl2溶液已过量
(5)16.7%
解析:混合物中组成(NH4)2SO4和NH4Cl,阳离子相同,因此应根据![]() 和Cl-的不同性质,将其中的一种沉淀下来,但不能用Ag+来沉淀Cl-,因为Ag2SO4微溶,当加入AgNO3沉淀Cl-时,部分
和Cl-的不同性质,将其中的一种沉淀下来,但不能用Ag+来沉淀Cl-,因为Ag2SO4微溶,当加入AgNO3沉淀Cl-时,部分![]() 也会沉淀下来,因此应用Ba2+将
也会沉淀下来,因此应用Ba2+将![]() 沉淀出来。由BaSO4的质量算出(NH4)2SO4的含量,计算方法为:m(BaSO4)=
沉淀出来。由BaSO4的质量算出(NH4)2SO4的含量,计算方法为:m(BaSO4)=![]() ×100%=16.7%。
×100%=16.7%。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目