摘要:取 6.60 g NaHCO3 和 Na2O2 的固体混合物.在密闭容器中加热到 250℃.经充分反应后排出气体.冷却后称得固体质量为 5.30 g.计算原混合物中 Na2O2 的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_337424[举报]
实验室需要250mL 0.5mol/L的稀硫酸溶液,现用密度为1.84g/mL,质量分数为98%浓硫酸配制;填空并请回答下列问题:
(1)请先通过计算(要有计算过程),再确定量取
(2)下列仪器中,不会用到的是
A.250mL容量瓶; B.500mL容量瓶; C.托盘天平; D.10mL量筒; E.玻棒;
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是
(4)容量瓶在使用前必须进行的操作是
(5)配制过程简述为以下各步:其正确的操作顺序为
(6)在配制过程中,定容时若俯视刻度线,则所配溶液的浓度偏
查看习题详情和答案>>
(1)请先通过计算(要有计算过程),再确定量取
6.8
6.8
mL浓硫酸.(2)下列仪器中,不会用到的是
B、C
B、C
A.250mL容量瓶; B.500mL容量瓶; C.托盘天平; D.10mL量筒; E.玻棒;
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是
胶头滴管、烧杯
胶头滴管、烧杯
.(4)容量瓶在使用前必须进行的操作是
查漏
查漏
.(5)配制过程简述为以下各步:其正确的操作顺序为
CDAGBEF
CDAGBEF
(填各步骤序号).A.冷却; B.洗涤; C.量取; D.溶解; E.定容; F.摇匀; G.移液(6)在配制过程中,定容时若俯视刻度线,则所配溶液的浓度偏
高
高
(填“高”或“低”); 若在滴加蒸馏水时,不慎超过了刻度线,应如何处理?重新配制溶液
重新配制溶液
.已知:5C2042-+2MnO4-+16H+=10CO2↑+2Mn2++8H20.现称取6.0g含H2C2O4?2H20、KHC2O4等的试样,加水溶解,配成250mL溶液.量取两份此溶液各25.00mL,分别置于两个锥形瓶中.
①第一份溶液中加入酚酞试液,滴加O.250mol/L NaOH溶液至20.00mL时,溶液由无色变为浅红色.
②第二份溶液中滴加O.100mol/L的酸性高锰酸钾溶液至16.00mL时,溶液颜色由无色变为紫红色.
原试样中H2C2O4?2H2O的质量分数为( )
①第一份溶液中加入酚酞试液,滴加O.250mol/L NaOH溶液至20.00mL时,溶液由无色变为浅红色.
②第二份溶液中滴加O.100mol/L的酸性高锰酸钾溶液至16.00mL时,溶液颜色由无色变为紫红色.
原试样中H2C2O4?2H2O的质量分数为( )
查看习题详情和答案>>
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.
(1)写出下列仪器的名称:
①
(2)仪器①~④中,使用时必须检查是否漏水的有
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有
查看习题详情和答案>>

(1)写出下列仪器的名称:
①
蒸馏烧瓶
蒸馏烧瓶
②冷凝管
冷凝管
③烧杯
烧杯
④容量瓶
容量瓶
(2)仪器①~④中,使用时必须检查是否漏水的有
④
④
(填序号)具体检查方法是往容量瓶中加入少量水,塞好瓶塞,用食指摁住瓶塞,另一只手托住瓶底,将容量瓶倒立,观察瓶塞周围是否有水漏出.如不漏水,将瓶正立,瓶塞旋转1800,重复上述操作
往容量瓶中加入少量水,塞好瓶塞,用食指摁住瓶塞,另一只手托住瓶底,将容量瓶倒立,观察瓶塞周围是否有水漏出.如不漏水,将瓶正立,瓶塞旋转1800,重复上述操作
.(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有
酒精灯、温度计
酒精灯、温度计
,将仪器补充完整后进行的实验操作的名称为:蒸馏或分馏
蒸馏或分馏
;使用时进水口为g
g
(填f或g).现需配制800mL 0.2mol/L NaOH溶液,某该同学用托盘天平称取6.4克NaOH固体,其中装置II是该同学转移溶液的示意图,该同学操作的错误是未用玻璃棒引流,称量NaOH应为8g
未用玻璃棒引流,称量NaOH应为8g
.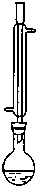 (2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:
(2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:①称取0.255g样品.
②将样品与25mL 4mol?L-lNaOH水溶液在100mL圆底烧瓶中混合,水浴加热l小时后停止加热(在如图所示装置中进行反应,发生的反应为:C6H5CH2Cl+NaOH→C6H5CH2OH+NaCl).
③在烧瓶中加入50mL 200/0HN03,混合均匀.
④将烧瓶中溶液全部转移到100mL容量瓶中,加水定容.
⑤从容量瓶中取出25.00mL溶液于锥形瓶中,加入6.25mL 0.100mol?L-1AgNO3溶液,振荡混合均匀.
⑥在锥形瓶中滴入几滴NH4Fe(SO4)2溶液作为指示剂,用0.0250mol?L-1 NHSCN溶液滴定剩余的AgNO3.
⑦重复⑤、⑥步骤三次,消耗0.0250mol?L1NH4SCN溶液的平均值为6.75mL.(已知:NH4CN+AgNO3=AgSCN↓+NH4NO3)
根据以上实验信息回答下列相关问题:
(1)上图中烧瓶上的冷凝管所起的作用是
冷凝回流作用
冷凝回流作用
.(2)步骤③所加硝酸的目的是
中和NaOH并使溶液呈酸性,防止下一步测定的干扰,
中和NaOH并使溶液呈酸性,防止下一步测定的干扰,
.(3)在步骤⑤操作中,可用
酸式滴定管
酸式滴定管
(填仪器名称)取6.25mL 0.1000mol?L-l的AgNO3溶液.(4)在步骤⑥操作中,判断达到滴定终点的现象是
溶液由无色变为红色,且半分钟内不褪色
溶液由无色变为红色,且半分钟内不褪色
.