网址:http://m.1010jiajiao.com/timu3_id_336891[举报]
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
 2009年10月15日新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:
2009年10月15日新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:(1)煤的汽化和液化可以提高燃料的利用率.
已知25℃,101kPa时:C(s)+1/2O2(g)=CO(g)△H=-126.4kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1
H2O(g)=H2O(l)△H=-44kJ?mol-1
则在25℃,101kPa时:C(s)+H2O(g)=CO(g)+H2(g)△H=
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g) Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263.
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值
②1100℃时测得高炉中,c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,则在这种情况下,该反应是否处于化学平衡状态
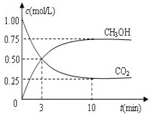
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.现向体积为1L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)=
②下列措施能使
| c(CH3OH) | c(CO2) |
A.升高温度 B.再充入H2 C.再充入CO2
D.将H2O(g)从体系中分离 E.充入He(g),使体系压强增大.

(1)写出甲试管中的主要化学反应方程式:___________________________________________。
(2)加入浓硫酸的目的是__________________________________________________________。
(3)试管乙中观察到的现象是______________________________________________________。
(4)在实验中球形管除起冷凝作用外,另一个重要作用是__________________________,其原因是______________________________。
(5)饱和碳酸钠溶液的作用是____________________________。
查看习题详情和答案>>
(1)写出甲试管中的主要化学反应方程式____________________________________________。
(2)加入浓硫酸的目的是____________________________________________________。
(3)试管乙中观察到的现象是_________________________________________________。
(4)在实验中球形干燥管除了起冷凝作用外,另一个重要作用是_________________________,其原理是________________________________________________________________。
(5)饱和碳酸钠溶液的作用是________________________________________________。
查看习题详情和答案>>