网址:http://m.1010jiajiao.com/timu3_id_33600[举报]
(11分)A、B两种物质都是由氢、氮、氧、钠四种元素中的三种元素所组成,在同温下,A溶液呈碱性而B溶液呈酸性。第一种组合中的A的浓溶液可以用来检验NH4+,请找出A和B可能的两种组合,并且要求当这两种组合中的B溶液pH相同时,第一种组合的B溶液中水的电离程度小于第二种组合的B溶液中水的电离程度。
(1)写出两种组合中A和B的化学式:(四种物质要各不相同,不考虑弱酸弱碱盐)
第一种组合:A是__________,B是_____________;
第二种组合:A是__________,B是_____________。
(2)说明pH相等时,第一种组合B溶液中水的电离程度比第二种组合B溶液中水的电离程度小的原因:____________________________________________________。
查看习题详情和答案>>A、B两种物质都是由氢、氮、氧、钠四种元素中的三种元素所组成,在同温下,A溶液呈碱性而B溶液呈酸性.第一种组合中的A的浓溶液可以用来检验NH![]() ,请找出A和B可能的两种组合,并且要求当这两种组合中的B溶液pH相同时,第一种组合的B溶液中水的电离程度小于第二种组合的B溶液中水的电离程度.
,请找出A和B可能的两种组合,并且要求当这两种组合中的B溶液pH相同时,第一种组合的B溶液中水的电离程度小于第二种组合的B溶液中水的电离程度.
(1)写出两种组合中A和B的化学式:(四种物质要各不相同,不考虑弱酸弱碱盐)
第一种组合:A是________,B是________;
第二种组合:A是________,B是________.
(2)说明pH相等时,第一种组合B溶液中水的电离程度比第二种组合B溶液中水的电离程度小的原因:_____________.
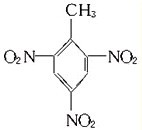
(1)写出由上述四种元素组成的可用作炸药的两种物质的结构简式:
①


②

(2)写出符合下列要求的物质的结构简式或分子式.①由上述四种元素中的三种组成的天然高分子的结构简式(任写一种)
②A、B两种共价化合物,它们均含上述四种元素,且互为同分异构体;它们的一分子中都含有两个碳原子,A可发生缩聚反应,B分子中含40个电子,且通常为中性,则A、B结构简式分别为:
A


B


(1)写出由上述四种元素组成的可用作炸药的两种物质的结构简式。
①________________________②________________________
(2)写出由上述四种元素中的两种组成的天然高分子的结构简式(任写一种物质)。
(3)由上述四种元素中的三种组成的天然高分子化合物A,是人体所需要的三大营养物质之一。它在人体中某种酶的作用下发生________反应(填反应类型)。写出其反应生成的最终产物的化学方程式:________________________。
(4)B、C为两种共价化合物,它们均含上述四种元素,且互为同分异构体;它们的一个分子中都含有两个碳原子,B可以发生缩聚反应,C分子中含有40个电子。C的结构简式为________,B与NaOH溶液反应的化学方程式为________________。
查看习题详情和答案>>(12分)
A.原子数相同、电子总数相同的分子,互称为等电子体。
Ⅰ.已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、6和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1 :2。
请回答:
(1)组成A分子的原子的元素符号是 ;已知E是有毒的有机物,E的熔、沸点比CH4的熔、沸点高,其主要原因是____________________________________。
(2)C的立体结构呈 ____ 形,该分子属于 分子(填“极性”或“非极性”);
(3)火箭中可充入四氧化二氮和D作为燃料反应生成氮气和水,该反应的化学方程式为_______ __________________。(不需要写反应条件)
Ⅱ.CO与N2互为等电子体。
(4)CO的总键能大于N2的总键能,但CO比N2容易参加化学反应。
根据下表数据,说明CO比N2活泼的原因是____________________________________。
| | | A-B | A=B | A≡B |
| CO | 键能(kJ/mol) | 357.7 | 798.9 | 1071.9 |
| 键能差值kJ/mol) | 441.2 273 | |||
| N2 | 键能(kJ/mol) | 154.8 | 418.4 | 941.7 |
| 键能差值kJ/mol) | 263.6 523.3 | |||
(6)Fe、Co、Ni等金属能与CO反应的原因与这些金属原子的电子层结构有关。
Ni原子的价电子排布式为 _____ 。Fe(CO)5常温下呈液态,熔点为
-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 ____(填晶体类型);Fe(CO)5是配合物,配体是__________ 。
B.茶中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素。某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
步骤1:称取500g干燥的茶叶,置于通风橱中,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后将200mL 1 mol·L-1盐酸加入灰中搅拌、过滤、洗涤。
步骤2:向步骤1所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH至6~7左右,使铝、铁元素以氢氧化物的形式完全沉淀,再加热煮沸30 min,加入7.95g无水碳酸钠,充分搅拌,待沉淀完全后,过滤,洗涤,过滤后得到滤液和沉淀。
步骤3:将步骤2所得的滤液稀释至500 mL,取其中的20.00 mL溶液以甲基橙作指示剂,用0.100mol·L-1的HCl标准溶液滴定,终点时消耗盐酸的体积为20.00mL,计算结果。
请回答下列问题:
步骤 1中,使茶叶灰化时需要用到三角架、泥三角、酒精喷灯、 ___、 ____ 等仪器。
步骤2中,改用试剂 _______ (写试剂名称)来调节pH将更为方便;判断沉淀已经洗净的方法是 。
步骤3中,滴定过程中,眼睛应注视 ____________________,被滴定的20 mL滤液中含CO32-的物质的量为 __ mol,试计算原500g茶叶中钙离子的质量分数为 _______ ,计算过程如下: 查看习题详情和答案>>