摘要:已知8%.7.16%.0.01%分别是同一条件下.同一浓度的三种酸溶液的电离度.若已知有如下反应: NaCN+HNO2==HCN+NaNO2 NaCN+HF==HCN+NaF NaNO2+HF==HNO2+NaF,在相同条件下.由此可判断得出的结论是: A.HF的电离度为8% B.HNO2的电离度为0.01% C.HCN的电离度为7.16% D.HNO2电离度比HCN大.比HF小
网址:http://m.1010jiajiao.com/timu3_id_332016[举报]
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题:(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、N
| H | + 4 |
| H | + 4 |
NH4Cl和NH3?H2O
NH4Cl和NH3?H2O
.(2)0.1mol?L-1的氨水与0.05mol?L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:
NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是
R2Z>RX>RY
R2Z>RX>RY
.(4)以石墨电极电解100mL 0.1mol?L-1CuSO4溶液.若阳极上产生气体的物质的量为0.01mol,则阴极上析出Cu的质量为
0.64
0.64
g.(5)向20mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=
0.2
0.2
mol?L-1.(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+
I2(g)?2HI(g)△H=-14.9kJ?mol-1),在恒温、恒容条件下,测得反应达
到平衡时的数据如下表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度(mol?L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
AC
AC
.A.α1+α2=1 B.2α2=α3 C.a+b=14.9 D.c1=c2=c3.
Ⅰ电离平衡常数(用K表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液 ②NaHCO3溶液 ③NaF溶液 ④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(2)25℃时,在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示 ,下列说法正确的是 .
,下列说法正确的是 .
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol?L-1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-akJ?mol-1,
②H+(aq)+OH-(aq)=H2O(l)△H=-bkJ?mol-1,
氢氟酸的电离方程式及热效应可表示为 .
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移 mol电子.
Ⅱ氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g) SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1
(1)试写出常温常压下化学平衡常数K的表达式:K= ;
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是 (选填编号).
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是 (选填编号).
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是 .
查看习题详情和答案>>
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(2)25℃时,在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示
 ,下列说法正确的是
,下列说法正确的是A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol?L-1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-akJ?mol-1,
②H+(aq)+OH-(aq)=H2O(l)△H=-bkJ?mol-1,
氢氟酸的电离方程式及热效应可表示为
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移
Ⅱ氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g)
 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1(1)试写出常温常压下化学平衡常数K的表达式:K=
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是
2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁?沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献.蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法.其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应
式为:2(-NH2)+H2SO4+2H+
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7.
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量.
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石.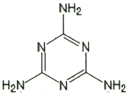
①三聚氰胺的结构如图所示,其化学式为
②下列关于三聚氰胺的说法中,正确的有
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入
查看习题详情和答案>>
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应
式为:2(-NH2)+H2SO4+2H+
| CuSO4 |
(NH4)2SO4
(NH4)2SO4
.Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7.
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量.
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为
(NH4)2SO4
(NH4)2SO4
.(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石.

①三聚氰胺的结构如图所示,其化学式为
C3H6N6
C3H6N6
,含氮量(氮元素的质量分数)为66.7%
66.7%
;②下列关于三聚氰胺的说法中,正确的有
AC
AC
;A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入
18.8
18.8
g的三聚氰胺就可使奶粉“达标”.Ⅰ.以硫铁矿为原料制取硫酸的生产中排出的废水对环境危害极大.酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表.
表1.几种砷酸盐的Ksp
表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=
Ⅱ.“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ?mol-1
③C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ?mol-1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
标准状况下的煤炭气(CO、H2)33.6L与氧气完全反应生成CO2和H2O,反应过程中转移
查看习题详情和答案>>
表1.几种砷酸盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As元素 |
| 浓度 | 28.42g/L | 1.6g?L-1 |
| 排放标准 | pH 6~9 | 0.5mg?L-1 |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
0.29
0.29
mol?L-1.(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=
c3(Ca2+)?c2 (AsO43-)
c3(Ca2+)?c2 (AsO43-)
,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,c(AsO43-)的最大是5.7×10-17
5.7×10-17
mol?L-1.Ⅱ.“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ?m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ?mol-1
③C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ?mol-1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
-524.8
-524.8
kJ?mol-1.标准状况下的煤炭气(CO、H2)33.6L与氧气完全反应生成CO2和H2O,反应过程中转移
3
3
mol e-.