摘要:根据物质的性质和用途.可将碱石灰.P2O5和CaCl2(固)归为一类.从以下选项中选出能与这三种物质归为一类的物质应该是( ) A.浓HNO3 B.NaCl C.NaHCO3 D.浓H2SO4
网址:http://m.1010jiajiao.com/timu3_id_331846[举报]
化学中用类比的方法可预测许多物质的性质.如根据H2+Cl2=2HCl推测:H2+Br2=2HBr.但类比是相对的,如根据2Na2O2+2CO2=2Na2CO3+O2类推:2Na2O2+2SO2=2Na2SO3+O2是错误的,应该为:Na2O2+SO2=Na2SO4.
(1)下列各组类比中正确的是 (填序号);
A.由NH4Cl
NH3↑+HCl↑ 推测:NH4I
NH3↑+HI↑
B.由2Fe+3Cl2═2FeCl3 推测:2Fe+3Br2═2FeBr3
C.由Na2SO3+2HCl=2NaCl+H2O+SO2↑ 推测:Na2SO3+2HNO3═2NaNO3+H2O+SO2↑
D.由I2易溶于KI溶液 推测:Cl2易溶于NaCl溶液
(2)由氧化铁与盐酸反应生成氯化铁和水,应用有关知识推断写出氧化亚铁与稀硝酸反应的化学方程式 ;
(3)电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-的化学方程式为:
CN-+ ClO-+ H2O= HCO3-+ N2+ Cl-,
配平该反应的化学方程式,在空格填上系数;
(4)(CN)2被称为拟卤素,它的阴离子CN-作为配体形成的配合物有重要用途.HgCl2和Hg(CN)2反应可制得Hg2Cl2 和(CN)2,该反应的氧化产物是 .
查看习题详情和答案>>
(1)下列各组类比中正确的是
A.由NH4Cl
| ||
| ||
B.由2Fe+3Cl2═2FeCl3 推测:2Fe+3Br2═2FeBr3
C.由Na2SO3+2HCl=2NaCl+H2O+SO2↑ 推测:Na2SO3+2HNO3═2NaNO3+H2O+SO2↑
D.由I2易溶于KI溶液 推测:Cl2易溶于NaCl溶液
(2)由氧化铁与盐酸反应生成氯化铁和水,应用有关知识推断写出氧化亚铁与稀硝酸反应的化学方程式
(3)电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-的化学方程式为:
配平该反应的化学方程式,在空格填上系数;
(4)(CN)2被称为拟卤素,它的阴离子CN-作为配体形成的配合物有重要用途.HgCl2和Hg(CN)2反应可制得Hg2Cl2 和(CN)2,该反应的氧化产物是
(1)某化学兴趣小组的同学为探究铝、铜和钛的金属活动性顺序,进行了如下实验:
①先用砂布将金属表面擦光亮。
②将大小厚薄相等的三种金属片分别放人盛有同浓度同体积盐酸的试管中,观察到如下现象:

依上表现象推断三种金属的活动性顺序为_______>_______>______。
(2)根据三种金属的性质或用途等回答下列问题:
①高层建筑常采用铝合金门窗而不采用铁门窗,原因是______________________________________。
②小林同学发现铜制眼镜框表面产生少量绿色物质,经查阅资料得知该物质为铜锈,又俗称铜绿,其主要成分是Cu2(OH)2CO3。用你学过的一种常见物质_____________(填名称)通过化学反应帮小林同学除去铜锈。
③钛和钛合金广泛用于火箭、航天飞机、船舶等,即使把它们放到海水中数年,取出后仍光亮如初,这说明金属钛具有很强的___________性。 查看习题详情和答案>>
①先用砂布将金属表面擦光亮。
②将大小厚薄相等的三种金属片分别放人盛有同浓度同体积盐酸的试管中,观察到如下现象:

依上表现象推断三种金属的活动性顺序为_______>_______>______。
(2)根据三种金属的性质或用途等回答下列问题:
①高层建筑常采用铝合金门窗而不采用铁门窗,原因是______________________________________。
②小林同学发现铜制眼镜框表面产生少量绿色物质,经查阅资料得知该物质为铜锈,又俗称铜绿,其主要成分是Cu2(OH)2CO3。用你学过的一种常见物质_____________(填名称)通过化学反应帮小林同学除去铜锈。
③钛和钛合金广泛用于火箭、航天飞机、船舶等,即使把它们放到海水中数年,取出后仍光亮如初,这说明金属钛具有很强的___________性。 查看习题详情和答案>>
 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含VA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)白磷单质的中P原子采用的轨道杂化方式是
sp3
sp3
;(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为
N>P>As
N>P>As
;(3)As原子序数为
33
33
,其核外M层和N层电子的排布式为3s23p63d104s24p3
3s23p63d104s24p3
;(4)NH3的沸点比PH3
高
高
(填“高”或“低”),原因是NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力
NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力
.PO43-离子的立体构型为
正四面体
正四面体
;(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13.硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因
第一步电离出的氢离子抑制第二步的电离
第一步电离出的氢离子抑制第二步的电离
;②硝酸比亚硝酸酸性强的原因
硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子
硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子
;(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为
| ||
| 2 |
| ||
| 2 |
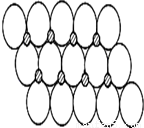
在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为
1.83×10-3
1.83×10-3
g (氧离子的半径为1.40×10-10m)氮化硅是一种超硬物质,抗腐蚀能力强,还能抗冷热冲击。工业上可用高纯硅与纯氮气在高温下反应制取。
(1)根据氮化硅的性质,推测其用途是____________(填序号)。
A.制造永久性模具
B.制汽轮机叶片
C.制石英玻璃
D.制造柴油机
(2)根据氮和硅在周期表中的位置,写出氮化硅的化学式:____________。
(3)氮化硅可被氢氟酸腐蚀,生成四氟化硅和氨。试写出该反应的化学方程式:__________________________________________________。
查看习题详情和答案>>
【化学--选修3:物质结构与性质】
VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含VA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)白磷单质的中P原子采用的轨道杂化方式是______;
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______;
(3)As原子序数为______,其核外M层和N层电子的排布式为______;
(4)NH3的沸点比PH3______(填“高”或“低”),原因是______.
PO43-离子的立体构型为______;
(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13.硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因______;
②硝酸比亚硝酸酸性强的原因______;
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为______
 查看习题详情和答案>>
查看习题详情和答案>>
VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含VA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)白磷单质的中P原子采用的轨道杂化方式是______;
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______;
(3)As原子序数为______,其核外M层和N层电子的排布式为______;
(4)NH3的沸点比PH3______(填“高”或“低”),原因是______.
PO43-离子的立体构型为______;
(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13.硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因______;
②硝酸比亚硝酸酸性强的原因______;
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为______
 查看习题详情和答案>>
查看习题详情和答案>>