题目内容
 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含VA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)白磷单质的中P原子采用的轨道杂化方式是
sp3
sp3
;(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为
N>P>As
N>P>As
;(3)As原子序数为
33
33
,其核外M层和N层电子的排布式为3s23p63d104s24p3
3s23p63d104s24p3
;(4)NH3的沸点比PH3
高
高
(填“高”或“低”),原因是NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力
NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力
.PO43-离子的立体构型为
正四面体
正四面体
;(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13.硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因
第一步电离出的氢离子抑制第二步的电离
第一步电离出的氢离子抑制第二步的电离
;②硝酸比亚硝酸酸性强的原因
硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子
硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子
;(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为
| ||
| 2 |
| ||
| 2 |
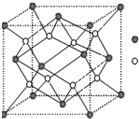
在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为
1.83×10-3
1.83×10-3
g (氧离子的半径为1.40×10-10m)分析:(1)白磷是正四面体结构,每个磷原子含有3个共价键和一个孤电子对,根据价层电子对确定其杂化方式;
(2)同一主族中,元素的第一电离能随着原子序数的增大而减小;
(3)砷是33号元素,M层排了18个电子,N层排了5个电子,据此写出核外M层和N层电子的排布式;
(4)同一主族元素的氢化物中,氢化物的沸点随着其相对分子质量的增大而增大,但含有氢键的氢化物沸点比不含氢键的高,根据价层电子对互斥理论确定其空间构型;
(5)含有相同的离子能抑制弱电解质的电离,硝酸与亚硝酸相比,存在一个N对O的配位键,因为这个配位键,使得N显更强的正电性,对羟基中H-O键的电子云的拉力更大,即极性更大,H更容易以质子的形式离去;
(6)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为
a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的
倍,根据图片知,每个氧化镍所占的面积=1.40×10-10m×1.40×10-10m×sin60°,每个氧化镍的质量=
g,每个氧化镍的质量乘以每平方米含有的氧化镍个数就是每平方米含有的氧化镍质量.
(2)同一主族中,元素的第一电离能随着原子序数的增大而减小;
(3)砷是33号元素,M层排了18个电子,N层排了5个电子,据此写出核外M层和N层电子的排布式;
(4)同一主族元素的氢化物中,氢化物的沸点随着其相对分子质量的增大而增大,但含有氢键的氢化物沸点比不含氢键的高,根据价层电子对互斥理论确定其空间构型;
(5)含有相同的离子能抑制弱电解质的电离,硝酸与亚硝酸相比,存在一个N对O的配位键,因为这个配位键,使得N显更强的正电性,对羟基中H-O键的电子云的拉力更大,即极性更大,H更容易以质子的形式离去;
(6)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为
| 1 |
| 2 |
| 2 |
| 74.7 |
| NA |
解答:解:(1)白磷分子中,每个磷原子含有3个共价键和一个孤电子对,所以其价层电子对是4,采取sp3杂化,
故答案为:sp3;
(2)N、P、As属于同一主族,且原子序数依次增大,原子序数越大,其最外层电子越容易失去,其电离电离能越小,所以这三种元素的第一电离能大小顺序是N>P>As,故答案为:N>P>As;
(3)砷的原子序数是33,M层排了18个电子,N层排了5个电子,所以其核外M层和N层电子的排布式为3s23p63d104s24p3,
故答案为:33,3s23p63d104s24p3;
(4)氨气的沸点高于高PH3,因为NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力,导致氨气的沸点比PH3高,PO43-离子价层电子对=4+
(5+3-4×2)=4,且没有孤电子对,所以其空间构型是正四面体,
故答案为:高,NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力,正四面体;
(5)①磷酸能分步电离,第一步电离出的氢离子抑制了第二步电离,所以H3PO4的K1远大于K2,
故答案为:第一步电离出的氢离子抑制第二步的电离;
②硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子,则酸性较大,
故答案为:硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子;
(6)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为
a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的
倍,所以其距离是
acm;
根据图片知,每个氧化镍所占的面积=1.40×10-10m×1.40×10-10m×sin60°,则每平方米含有的氧化镍个数=
,每个氧化镍的质量=
g,所以每平方米含有的氧化镍质量=
×
=
=1.83×10-3,
故答案为:
a,
=1.83×10-3.
故答案为:sp3;
(2)N、P、As属于同一主族,且原子序数依次增大,原子序数越大,其最外层电子越容易失去,其电离电离能越小,所以这三种元素的第一电离能大小顺序是N>P>As,故答案为:N>P>As;
(3)砷的原子序数是33,M层排了18个电子,N层排了5个电子,所以其核外M层和N层电子的排布式为3s23p63d104s24p3,
故答案为:33,3s23p63d104s24p3;
(4)氨气的沸点高于高PH3,因为NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力,导致氨气的沸点比PH3高,PO43-离子价层电子对=4+
| 1 |
| 2 |
故答案为:高,NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力,正四面体;
(5)①磷酸能分步电离,第一步电离出的氢离子抑制了第二步电离,所以H3PO4的K1远大于K2,
故答案为:第一步电离出的氢离子抑制第二步的电离;
②硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子,则酸性较大,
故答案为:硝酸中N呈+5价,N-O-H中O的电子更向N偏移,导致其越易电离出氢离子;
(6)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为
| 1 |
| 2 |
| 2 |
| ||
| 2 |
根据图片知,每个氧化镍所占的面积=1.40×10-10m×1.40×10-10m×sin60°,则每平方米含有的氧化镍个数=
| 1 |
| 1.40×10-10m×1.40×10-10m×sin60° |
| 74.7 |
| NA |
| 74.7 |
| NA |
| 1 |
| 1.40×10-10m×1.40×10-10m×sin60° |
| 74.7 |
| 6.02×1023×(2×1.40×10-10)2Sin600 |
故答案为:
| ||
| 2 |
| 74.7 |
| 6.02×1023×(2×1.40×10-10)2Sin600 |
点评:本题考查较综合,涉及电子排布式的书写、杂化方式的判断、晶胞的计算等知识点,难度较大,难点是晶胞的计算,注意(6)中氧化镍化学式的平面结构是平行四边形,而不是三角形,为易错点.

练习册系列答案
相关题目
【化学--选修3:物质结构与性质】
已知:①A的简单阴离子核外有2个电子,B元素原子最外层电子数是内层电子数的3倍,E原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于分子晶体,F元素原子序数为26.
②X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
回答下列问题:
(1)B元素原子核外已成对电子数是未成对电子数的 倍.
(2)X、Y、Z的电负性从大到小的顺序为 (用元素符号表示).
(3)分子式为A2B、A2E的两种物质中 更稳定(用化学式表示),原因是 .
(4)X的氯化物的熔点比Y的氯化物的熔点 ,原因是 .
(5)F的氯化物FCl3与KSCN溶液反应显红色,该反应的离子方程式为 .等电子体指的是原子总数相同.价电子总数相同的分子.离子或基团,据此定义写出离子SCN-的一种等电子体 .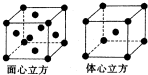
(6)F的一种常见配合物F(CO)3常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断F(CO)3的晶体类型为 .F元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示.在面心立方晶胞中F原子的配位数为 ,体心立方晶胞的密度可表示为 .(F的原子半径为r)
已知:①A的简单阴离子核外有2个电子,B元素原子最外层电子数是内层电子数的3倍,E原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于分子晶体,F元素原子序数为26.
②X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
(1)B元素原子核外已成对电子数是未成对电子数的
(2)X、Y、Z的电负性从大到小的顺序为
(3)分子式为A2B、A2E的两种物质中
(4)X的氯化物的熔点比Y的氯化物的熔点
(5)F的氯化物FCl3与KSCN溶液反应显红色,该反应的离子方程式为

(6)F的一种常见配合物F(CO)3常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断F(CO)3的晶体类型为
【化学 ——选修3:物质结构】(15分)
氮元素可形成卤化物、叠氮化物及络合物等。
(1)NF3构型为三角锥形,沸点为-129 ℃;可在铜 催化作用下由F2和过量NH3反应得到。NF3属于________晶体.
催化作用下由F2和过量NH3反应得到。NF3属于________晶体.
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N。
①与N互为等电子体的分子、离子有______、________(各举1例),由此可推知N的空间构型是______形。
②叠氮化物、氰化物能与Fe3+、Cu2+及Co3+等形成络合物,如Co[(N3)(NH3)5]SO4、[Fe(CN)6]4-。写出钴原子在基态时的价电子排布式:__________。如Co[(N3)(NH3)5]SO4、中钴的配位数为________,CN-中C原子的杂化类型是________。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)===2Na(l)+3N2(g),有关说法正确的是________(选填序号)。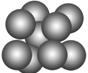
| A.NaN3与KN3结构类似,前者晶格能较小 |
| B.第一电离能(I1):N>P>S |
| C.钠晶胞结构如图,该晶胞分摊2个钠原子 |
| D.常温下,氮气很稳定,是因为氮的电负性小 |